
La transmutación es el acto de cambiar una sustancia, tangible o intangible, de una forma o estado a otra. Para los alquimistas de antaño, esto significaba la conversión de una sustancia física en otra, especialmente de metales básicos como el plomo en valiosa plata y oro. Para los científicos modernos, esto significa la transformación de un elemento en otro mediante una o una serie de desintegraciones o reacciones nucleares.
Aunque la gente trabajaba con el oro, la plata, el cobre, el hierro, el estaño, el plomo, el carbono, el azufre y el mercurio en la antigüedad, tenía pocos conocimientos de química y podía escribir poco sobre ella. En esta época la química era un arte, no una ciencia. Los egipcios fueron los primeros en producir una amplia documentación escrita sobre los procedimientos químicos, a principios de la era cristiana, y Egipto es generalmente identificado como la cuna de la química. Estos escritos indican que el desarrollo de métodos para transmutar una sustancia en otra fue uno de los principales objetivos iniciales de sus investigaciones. Durante los varios cientos de años que siguieron a estos escritos, los alquimistas intentaron desarrollar esquemas para transmutar los metales comunes en oro y plata mediante diversas manipulaciones químicas de mezclas y destilaciones. Los alquimistas se vieron estimulados por lo que parecía ser un cierto éxito -por ejemplo, la producción de cantidades muy pequeñas de oro a partir de mineral de plomo mediante sus procedimientos químicos. (Este oro estaba indudablemente presente en cantidades mínimas en los minerales originales y no fue producido por transmutación). La última locura de los alquimistas surgió durante la Edad Media con la búsqueda de la piedra filosofal, una sustancia que podía mezclarse con metales comunes y, mediante la purificación, convertirlos en oro. Nunca se encontró.
Debido a que cada elemento tiene un número diferente pero fijo de protones en el núcleo del átomo, que es el número atómico, la transmutación de un elemento químico en otro implica cambiar ese número. Una reacción nuclear de este tipo requiere millones de veces más energía que la disponible a través de las reacciones químicas. Por lo tanto, el sueño del alquimista de transmutar el plomo en oro nunca fue alcanzable químicamente.
Aunque los alquimistas no lograron encontrar un método para la transmutación de los metales comunes en metales preciosos, de sus esfuerzos surgieron varios procesos químicos importantes. Por ejemplo, extrajeron metales de las menas; produjeron una serie de ácidos y bases inorgánicas que posteriormente adquirieron importancia comercial; y desarrollaron las técnicas de fusión, calcinación, disolución, filtración, cristalización, sublimación y, sobre todo, destilación. Durante la Edad Media, comenzaron a intentar sistematizar los resultados de sus primitivos experimentos y sus fragmentos de información para explicar o predecir las reacciones químicas entre las sustancias. Así apareció la idea de los elementos químicos y las primeras formas primitivas de la Tabla Periódica química.
Irónicamente, las transmutaciones nucleares estaban teniendo lugar prácticamente bajo las narices de los alquimistas (o bajo sus pies), pero no tenían ni los métodos para detectar ni los conocimientos para utilizar estos sucesos. El descubrimiento del proceso de transmutación nuclear estuvo estrechamente relacionado con el descubrimiento de la radiactividad por Henri Becquerel en 1896. Las transmutaciones nucleares se producen durante la desintegración radiactiva espontánea del torio y el uranio naturales (números atómicos 90 y 92, respectivamente) y la

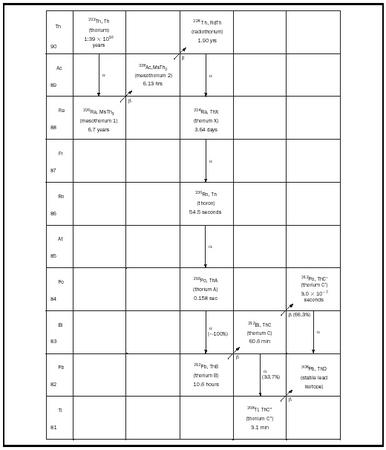
productos hijos de su desintegración, es decir, la serie de desintegración natural. Como ejemplo, la serie de desintegración del 232 Th se muestra en la figura 1. El superíndice 232 representa la masa atómica, que es el número total de protones y neutrones en el núcleo del átomo. En esta serie de desintegración, un núcleo de 232 Th comienza el proceso emitiendo espontáneamente una partícula α (un núcleo de He que contiene dos protones y dos neutrones). Esta reacción transmuta el núcleo de Th en un núcleo con dos protones y dos neutrones menos, el 228 Ra. A continuación, el núcleo de 228 Ra emite espontáneamente una partícula β (un electrón), que convierte un neutrón del núcleo en un protón, elevando el número atómico del núcleo resultante en uno sin que cambie la masa atómica, dando lugar a 228 Ac. Esta secuencia de desintegraciones α y β sucesivas continúa de un elemento a otro hasta que se produce el núcleo estable de 208 Pb (véase la figura 1). También existen otras dos cadenas de desintegración naturales, una que comienza con el 235 U (la serie del actinio) y otra que comienza con el 238 U (la serie del uranio). Además de estas tres series de desintegración, existen en la naturaleza otros catorce isótopos radiactivos, que van desde los 40 K hasta los 190 Pt, que se transmutan por desintegración en elementos estables.
La idea de la transmutación de los elementos en las cadenas de desintegración naturales no acompañó al descubrimiento de la radiactividad por parte de Becquerel. Sin embargo, Marie y Pierre Curie ampliaron las investigaciones de Becquerel utilizando una variedad de
Minerales de U y descubrieron que las propiedades radiactivas no eran función de las formas físicas o químicas del uranio, sino propiedades del propio elemento. Utilizando métodos de separación química, en 1898 aislaron dos nuevas sustancias radiactivas asociadas a los minerales de U y las denominaron polonio y radio. En 1902 Ernest Rutherford y Frederick Soddy explicaron la naturaleza del proceso que ocurre en las cadenas de desintegración natural como las desintegraciones radiactivas del U y el Th para producir nuevas sustancias por transmutación.
Lord Rutherford y su grupo de científicos fueron los primeros en producir y detectar transmutaciones nucleares artificiales en 1919. Bombardeó nitrógeno en el aire con las partículas α emitidas en la desintegración del 214 Po. La reacción de transmutación implicaba la absorción de una partícula α por los 14 núcleos de N para producir 17 O y un protón (un núcleo de hidrógeno). Esta reacción puede escribirse como
14 N + 4 He → 17 O + 1 H
Lord Rutherford pudo detectar e identificar los protones producidos en esta reacción nuclear y demostrar así el proceso de transmutación.
Hasta 1934, sólo se disponía de elementos radiactivos de origen natural para su estudio. Sin embargo, en enero de ese año, Irene Curie (hija de Marie Curie) y Frédéric Joliot informaron de que muestras de boro y aluminio se hacían radiactivas bombardeándolas con partículas α de polonio para producir los dos nuevos productos radiactivos, 13 N y 30 P respectivamente. Este descubrimiento estableció los nuevos campos de la química nuclear y la radioquímica y desencadenó su rápido crecimiento.
Con el desarrollo de los reactores nucleares y de los aceleradores de partículas cargadas (comúnmente denominados «destructores de átomos») durante la segunda mitad del siglo XX, la transmutación de un elemento en otro se ha convertido en algo habitual. De hecho, se han producido unas dos docenas de elementos sintéticos con números atómicos superiores al uranio natural mediante reacciones de transmutación nuclear. Así, en principio, es posible alcanzar el sueño del alquimista de transmutar el plomo en oro, pero el coste de producción mediante reacciones de transmutación nuclear superaría con creces el valor del oro.