A pszeudofakikus cisztoid makulaödéma (CME), más néven Irvine-Gass-szindróma fájdalommentes látásvesztéssel jár, és jellemzően 4-6 héttel a szürkehályogműtét után jelentkezik, bár a szövődmény kockázati tényezői gyakran már jóval korábban azonosíthatók. A CME fokozott kockázatának kitett betegek közé tartoznak a retinopátia nélküli cukorbetegek, a retinopátiás cukorbetegek (relatív kockázat 1,80 és 6,23), az epiretinalis membránnal kezelt betegek (RR 5.60) vagy uveitis (RR 2,88), valamint azok, akiknek retinavéna elzáródása van (RR 4,47).1
A CME szempontjából fokozott kockázatnak kitett betegek felvilágosítása a beavatkozás előtt fontos, mivel segít enyhíteni a megdöbbenésüket, ha a szövődmény bekövetkezik. Bizonyos intraoperatív szövődmények, mint például a hátsó kapszulaszakadás és a visszamaradt lencseanyag, szintén ismert, hogy növelik a CME előfordulási gyakoriságát.2 Amennyiben a betegnél a fentiek bármelyikét tapasztalja, a posztoperatív időszakban gyakori tágítás javallott lehet a CME jeleinek észlelése érdekében.
A következőkben néhány gyöngyszem, amit szem előtt kell tartania, amikor a szürkehályogműtétes betegeket komanizál.
RED FLAGS
A posztoperatív CME feltételezett etiológiai tényezői közé tartozik a gyulladás, a vitreomacularis trakció és az érrendszeri instabilitás. Az elsődleges etiológiának a műtéti manipuláció következtében a vizes és üvegtestben lévő szabályozatlan gyulladásos mediátorok tűnnek. Ezek a mediátorok (pl. leukotriének és prosztaglandinok) megbontják a vér-vakózus és a vér-retina gátakat, ami fokozott permeabilitáshoz vezet.3 A CME tipikus kezdetének időzítése annak tudható be, hogy mennyi időbe telik, amíg ezek a gyulladásos mediátorok az elülső szegmentumból a szem hátsó részébe jutnak.
A CME gyanúját a csökkent látásélesség vagy metamorfopszia kelti, amely nem magyarázható a szürkehályogműtéthez kapcsolódó egyéb okokkal, beleértve a maradék fénytörési hibát, a szaruhártya ödémát, a lencse hibás elhelyezkedését vagy a hátsó kapszula opakizációját.
A vizuálisan jelentős CME viszonylag ritka, a szemek 0,1-3,5%-ában fordul elő szürkehályogműtétet követően.4-6 A nem vizuálisan jelentős makulaödéma sokkal gyakoribb. Az OCT-vel vizsgált szemek 3-41%-ában és a fluoreszcein angiográfiával vizsgált szemek 20-55%-ában fordul elő.7
A páciens látótávolsága és tünetei határozzák meg az OCT-képalkotás szükségességét. A homályos látás egyéb leletek hiányában gondos tágított szemfenékvizsgálatot és makula OCT-t igényel (1. ábra). Az összes beteg rutinszerű képalkotása azonosíthat néhány tünetmentes CME-t, ami szükségtelen kezeléshez és a beteg szorongásához vezethet.
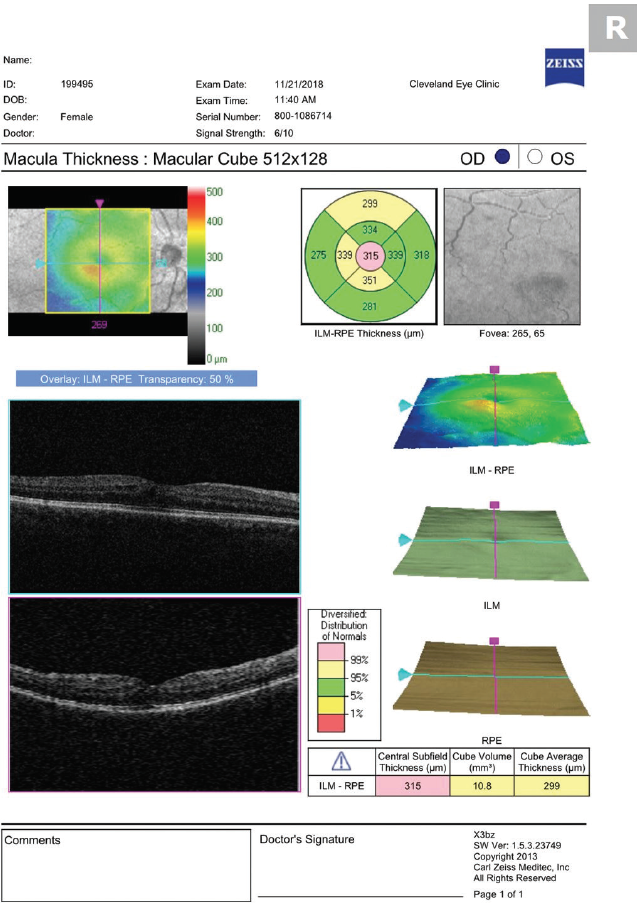
1. ábra. A szürkehályogműtét után 30 nappal végzett OCT enyhe CME-t mutat.
A CME MEGELŐZÉSE
Nincs konszenzus a CME megelőzésének vagy kezelésének optimális szükségességét illetően. A szürkehályogműtét előtti profilaktikus kezelés lokális nem szteroid gyulladásgátlóval (NSAID) csökkentette a CME előfordulását posztoperatívan; azonban a fellépő CME vizuális hatásai hosszú távon (>3 hónap) jelentéktelenek voltak.8
A közelmúltban a 9%-os dexametazon intraokuláris szuszpenzió (Dexycu, Eyepoint Pharmaceuticals) megkapta az FDA engedélyét az írisz mögé történő injekciózásra a szürkehályogműtét idején. Ez a készítmény biztonságosnak és hatékonynak bizonyult a szürkehályogműtét után fellépő gyulladás kezelésében, és alternatívája lehet a posztoperatív szteroidcsepp-instillációnak.9
A posztoperatív helyi gyulladáscsökkentő gyógyszerek profilaktikusan csökkentik a CME előfordulását. Egy 30 randomizált klinikai vizsgálat elemzése, amely nem cukorbetegek komplikációmentes szürkehályogműtétjét foglalta magában, kimutatta, hogy a posztoperatív helyi NSAID-ok jelentősen csökkentették a CME kialakulásának esélyét a posztoperatív helyi kortikoszteroidokhoz képest.10 Ez az elemzés azt is megállapította, hogy a kortikoszteroidok és NSAID-ok kombinációja jobb volt, mint a helyi kortikoszteroidok önmagukban.
Ha a betegnél a profilaktikus kezelés ellenére CME alakul ki, az állapot általában kezelhető helyi gyógyszerekkel. Bár az ödéma gyakran több hónap alatt magától megszűnik, a helyi NSAID-terápia hatékonyan csökkenti az OCT-vel kimutatott CME-t, és a placebóhoz képest felgyorsíthatja a látás helyreállítását a műtét után.11 A kortikoszteroid és az NSAID kombinációja szintén jobbnak tűnik, mint bármelyik gyulladáscsökkentő gyógyszer önmagában. Egy vizsgálatban a Snellen VA átlagos javulása 3 hónap alatt 1,6 vonal volt a NSAID-ot kapó betegeknél, 1,1 vonal a szteroidot kapó betegeknél és 3,8 vonal a kombinációt kapó betegeknél.12
Praxisunkban prednizolon-acetát 1%-ot és ketorolak 0,5%-ot írunk fel napi négyszeri alkalmazásra a CME megszűnéséig, majd ezt követően 3 hetes leépítés következik. Mindkettőt a retinacsoport, amellyel együtt dolgozunk, ajánlása szerint csapoljuk (1 hétig naponta háromszor, majd 1 hétig naponta kétszer, majd 1 hétig naponta egyszer). Ne ijedjen meg, ha a CME súlyossága közvetlenül a helyi kezelés megkezdése után romlik. Az ödéma késleltetett kialakulásához hasonlóan (feltételezhetően azért, mert a gyulladásos mediátoroknak időbe telik, amíg az elülső szegmentumból a retinába jutnak), a gyógyszereknek is időbe telik, amíg a szemfelszínről a retinába jutnak (2. és 3. ábra).
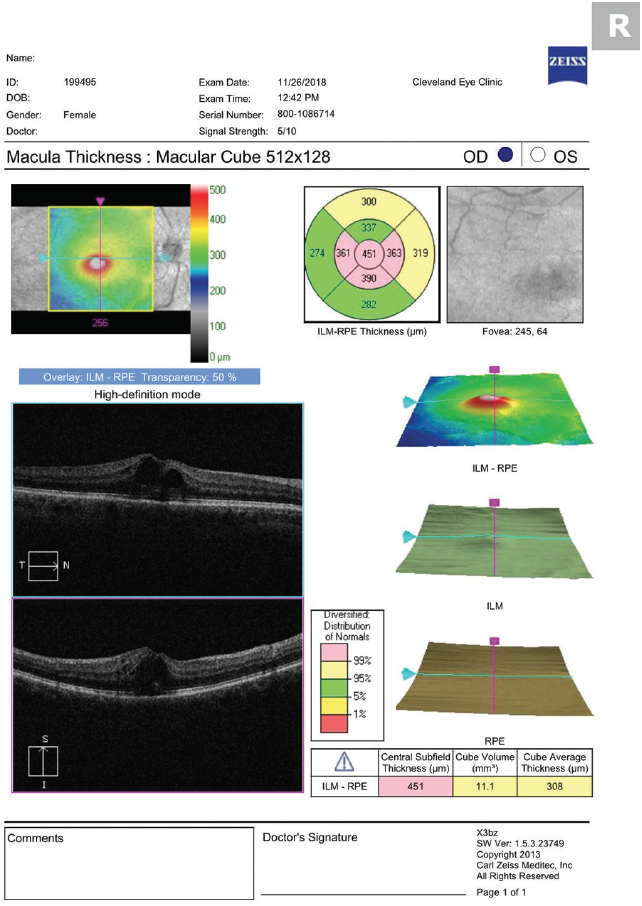
2. ábra. A prednizolon-acetát és ketorolak napi négyszeres kezelés megkezdése után 5 nappal végzett OCT a CME romlását mutatja.
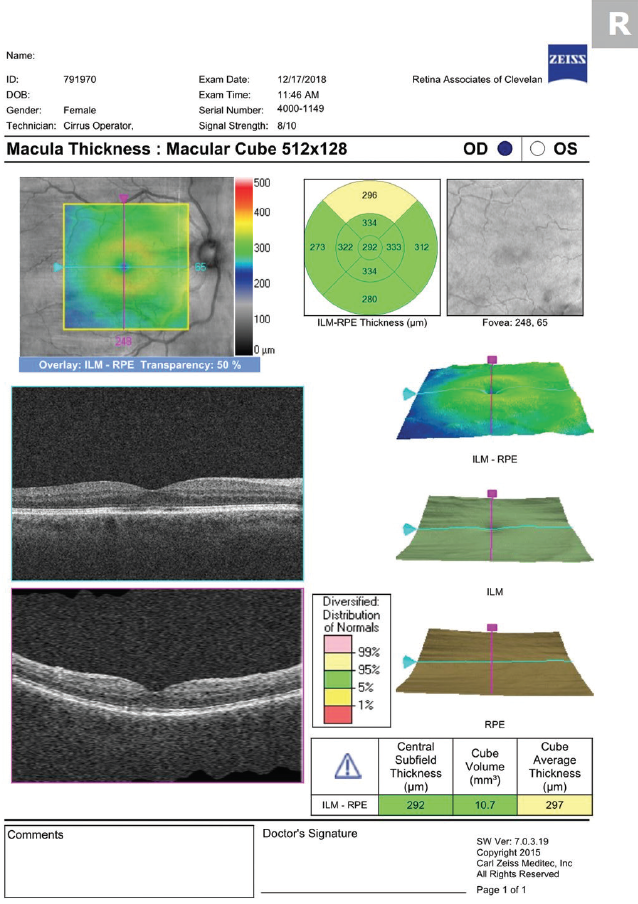
3. ábra. A kezelés megkezdése után 1 hónappal végzett OCT a CME feloldódását mutatja.
A visszahúzódó CME gyakran további beavatkozást igényel a látás helyreállításához. Ha a lokális kezelést követő 1 hónapon belül nem következik be strukturális (OCT-lelet) és funkcionális (VA) javulás, retina szakorvoshoz kell fordulni. A periocularis szteroidinjekciók (sub-Tenon és retrobulbaris) bizonyítottan csökkentik az ödémát és javítják a látótávolságot a helyi kezelésre refrakter CME-ben.13 Az intraocularis szteroidinjekciók és a kiterjesztett hatóanyag-leadású intravitreális implantátumok szintén javították a krónikus CME-ben szenvedő betegek eredményeit.14
A VEGF-ellenes injekciók szintén előnyösnek bizonyultak a krónikus CME kezelésében. Egy multicentrikus retrospektív vizsgálat szerint a refrakter CME-ben szenvedő, legalább egy bevacizumab (Avastin, Genentech) intravitreális injekcióval kezelt szemek 72%-ánál javult a látásélesség és csökkent az átlagos centrális makulavastagság 12 hónap után.15
A CME kezeléséhez bizonyos esetekben sebészeti módszereket kell alkalmazni. Például a visszamaradt lencseanyag sebészi eltávolítására lehet szükség a visszamaradt CME megoldásához. A pars plana vitrectomia szintén jobb látási eredményeket eredményezett olyan CME esetében, amely nem reagált a gyógyszeres kezelésre16.
MUTATKOZÓK
A szürkehályogműtéten átesett betegek komanagementje során érdemes felismerni a gyakori szövődményeket, például a CME-t, és tudni, hogyan kell eljárni, ha ezeket észleljük.
Összefoglalva, a kockázatos betegeket (cukorbetegségben, epiretinalis membránban, uveitisben vagy retinavéna elzáródásban szenvedők) már a műtét előtt azonosítani kell. Legyen tisztában az intraoperatív szövődményekkel is, amelyek növelhetik a CME kockázatát (pl. hátsó kapszularuptúra, visszamaradt lencsetöredékek). Zárja ki a posztoperatív homályosság egyéb okait, és végezzen gondos tágító vizsgálatot és makula OCT-t a CME azonosítására. Tájékoztassa és nyugtassa meg a beteget, hogy a CME kezelhető állapot. Kezelje helyileg NSAID-okkal és szteroidokkal, és további beavatkozás céljából utalja retina szakorvoshoz, ha a CME makacsul fennáll.
1. Henderson BA, Kim JY, Ament CS, Ferrufino-Ponce ZK, Grabowska A, Cremers SL. Klinikai pszeudofakikus cisztoid makulaödéma. A kialakulás kockázati tényezői és a kezelés utáni időtartam. J Cataract Refract Surg. 2007;33(9):1550-1558.
2. Kim SJ, Belair ML, Bressler NM, et al. A módszer a szürkehályogműtét utáni makulaödéma jelentésére optikai koherencia tomográfia segítségével. Retina. 2008;28(6):870-876.
3. Benitah NR, Arroyo JG. Pszeudofakikus cisztoid makulaödéma. Int Ophthalmol Clin. 2010;50(1):139-153.
4. Powe NR, Schein OD, Gieser SC, et al. Synthesis of the literature on visual acuity and complications following cataract extraction with intraocular lens implantation. Cataract Patient Outcome Research Team. Arch Ophthalmol. 1994;112(2):239-252.
5. Greenberg PB, Tseng VL, Wu WC, et al. Prevalence and predictors of ocular complications associated with cataract surgery in United States veterans. Ophthalmology. 2011;118(3):507-514.
6. Clark A, Morlet N, Ng JQ, et al. Whole population trends in complications of cataract surgery over 22 years in Western Australia. Ophthalmology. 2011;118(6):1055-1061.
7. Bélair ML, Kim SJ, Thorne JE, et al. A cisztoid makulaödéma előfordulása szürkehályogműtét után uveitiszes és uveitisz nélküli betegeknél optikai koherencia tomográfia segítségével. Am J Ophthalmol. 2009;148(1):128-135.
8. Grzybowski A, Kim SJ. Kortikoszteroidok helyettesítése nem szteroid gyulladáscsökkentőkkel: indokolja-e a bizonyítékokon alapuló orvoslás? J Cataract Refract Surg. 2016;42(3):510-511.
9. Donnenfeld E, Holland E. Dexametazon intrakamerális hatóanyag-leadó szuszpenzió a szürkehályogműtéthez társuló gyulladás kezelésére: randomizált, placebokontrollált, III. fázisú vizsgálat. Ophthalmology. 2018;125(6):799-806.
10. Heier JS, Topping TM, Baumann W, et al. Ketorolac versus prednizolon versus kombinált terápia az akut pszeudofakikus cisztoid makulaödéma kezelésében. Ophthalmology. 2000;107(11):2034-2039.
11. Kim SJ, Schoenberger SD, Thorne JE, Ehlers JP, Yeh S, Bakri SJ. Helyi nem-szteroid gyulladáscsökkentők és a szürkehályog műtét: az Amerikai Szemészeti Akadémia jelentése. Ophthalmology. 2015;122(11):2159-2168.
12. Shelsta HN, Jampol LM. A pszeudofakikus cisztoid makulaödéma farmakológiai terápiája: 2010-es frissítés. Retina. 2011;31(1):4-12.
13. Benhamou N, Massin P, Haouchine B, Audren F, Tadayoni R, Gaudric A. Intravitreális triamcinolon refrakter pszeudofakikus makulaödéma kezelésére. Am J Ophthalmol. 2003;135(2):246-249.
14. Bellocq D, Korobelnik JF, Burillon C, et al. Effectiveness and safety of dexamethasone implants for post-surgical macular oedema including Irvine-Gass syndrome: the EPISODIC study. Br J Ophthalmol. 2015;99(7):979-983.
15. Arevalo JF, Maia M, Garcia-Amaris RA, et al; Pan-American Collaborative Retina Study Group. Intravitreal bevacizumab for refractory pseudophakic cystoid macular edema: The Pan-American Collaborative Retina Study Group results. Ophthalmology. 2009;116:1481-1487.
16. Cardone S, et al. The role of pars plana vitrectomy for pseudophakic cystoid macular edema. Invest Ophthalmol Vis Sci. 2003;44(7):3012.

Charles A. Roseman, OD
- Cleveland Eye Clinic, Ohio
- [email protected]
- Financial disclosure: None