Caratteristiche tipiche
La RSTS è caratterizzata da un lento sviluppo di altezza e peso, microcefalia, caratteristiche facciali dismorfiche, pollice largo e dita grandi. Lo sviluppo prenatale è normale, con parametri di crescita medi o quasi normali alla nascita. I grafici di crescita si avvicinano tipicamente ai limiti inferiori della normalità nel primo periodo postnatale, riflettendo principalmente l’ipo-alimentazione esacerbata dal reflusso gastro-esofageo. Successivamente, la tendenza al sovrappeso o all’obesità (prima nei maschi che nelle femmine) può essere osservata durante l’adolescenza. Tabelle di crescita specifiche e recentemente riviste sono essenziali per una valutazione appropriata della crescita degli individui affetti. Le caratteristiche facciali sono caratterizzate principalmente da un’attaccatura dei capelli frontale bassa, sopracciglia arcuate/spesse, abbassamento delle fessure palpebrali, un naso a becco sporgente con columella al di sotto delle alae nasi, orecchie displasiche e di basso profilo, un palato arcuato, micrognazia lieve, anomalie dentali (conformazione alterata, malocclusione e sovraffollamento dei denti) e un sorriso atipico (“smorfie”) con occhi quasi completamente chiusi (Figura 1). I piedi e le mani presentano tipicamente un primo dito allargato e clinodattilia del quinto dito (Figura 2), mentre la polidattilia con pollici bifidi e prime dita dei piedi si osserva raramente. Altre anomalie scheletriche includono pollici abdotti, anomalie vertebrali, lassità legamentosa, grave e prolungata infiammazione asettica della testa del femore, anomalie simili alla malattia di Perthes (3%), e occasionalmente l’epifisi femorale capitale scivolata. In particolare, è stato riportato un alto rischio di anomalie vertebrali cervicali (instabilità di C1-C2, os odontoideum, ipoplasia del dens, fusione delle vertebre cervicali), con possibile stenosi alla giunzione craniovertebrale, che può causare mielopatia cervicale. Problemi neuroradiologici complessi, tra cui la disgenesia del corpo calloso (17%), la malformazione di Chiari tipo I con o senza siringomielia, la malformazione di Dandy Walker e l’idrocefalo, e il tethered cord sono stati segnalati e sono ancora sotto indagine. Anomalie cerebrovascolari come la dissezione spontanea delle arterie sopraaortiche e l’infarto cerebrale dovuto alla dissezione dell’aneurisma dell’arteria cerebrale anteriore sono stati anche segnalati. Tuttavia, qualsiasi organo può essere colpito nei pazienti RSTS. Possibili malformazioni, problemi medici e complicazioni includono (Tabella 1):
-
sordità conduttiva e/o neurosensoriale, infezioni ricorrenti dell’orecchio medio, infezioni respiratorie ricorrenti, immunodeficienze ;
-
anomalie non specifiche dell’elettroencefalogramma (EEG) (57-66%) e convulsioni (25%) ;
-
cataratta, coloboma unilaterale o bilaterale dell’iride/retina/nervo ottico (9-11%), glaucoma, ostruzioni del dotto lacrimale (38-47%), errori di rifrazione (41-56%) e strabismo (60-71%). Inoltre, Jacobs et al. hanno descritto per la prima volta l’avascolarità periferica con l’angiografia fluoresceinica nel 2012 ;
-
problemi dentali: cuspidi talonali (73%), ipoplasia dello smalto, e numero di denti anomalo ;
-
malattie cardiache congenite: difetto del setto atriale, difetto del setto ventricolare, dotto arterioso pervio, coartazione dell’aorta, stenosi polmonare, valvola aortica bicuspide, pseudotrunco, stenosi aortica, destrocardia, anelli vascolari e disturbi della conduzione (24-38%) . È stata riportata anche un’associazione occasionale di cuore sinistro ipoplasico con RSTS;
-
malformazioni renali (52%) e criptorchidismo (78-100%);
-
disturbi endocrini: ipotiroidismo congenito, ipoplasia tiroidea, deficit di GH e ipoplasia ipofisaria;
-
disturbi gastrointestinali: reflusso gastroesofageo, costipazione (40-74%) e megacolon/malattia di Hirschsprung ;
-
apnea ostruttiva del sonno, complicazioni da anestesia e intubazione ;
-
problemi della pelle tra cui pilomatrixomi, unghie incarnite, paronichia e tendenza a formare cheloidi (24%) ;
-
tumori, in particolare di origine neurale e dello sviluppo (neuroblastoma, medulloblastoma, oligodendroglioma, meningeoma, feocromocitoma, rabdomiosarcoma, leiomiosarcoma, seminoma, odontoma, coristoma e pilomatrixomi. Sono stati riportati anche leucemia e linfoma;
-
hirsutism
Figure 1 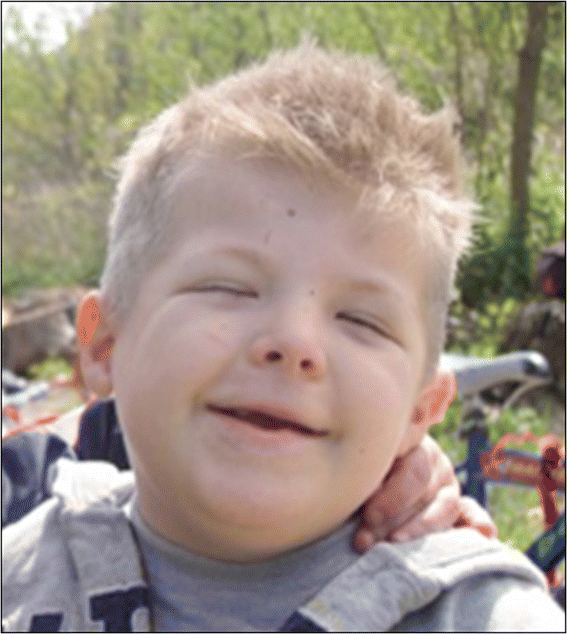
Typical facies of a RSTS patient, including arched eyebrows, slanted palpebral fissures, protruding beaked nose with columella below alae nasi, arched palate, mild micrognathia, labial commissures facing upward, teeth anomalies, and an atypical smile (“grimacing”) with nearly completely closed eyes.
Figure 2 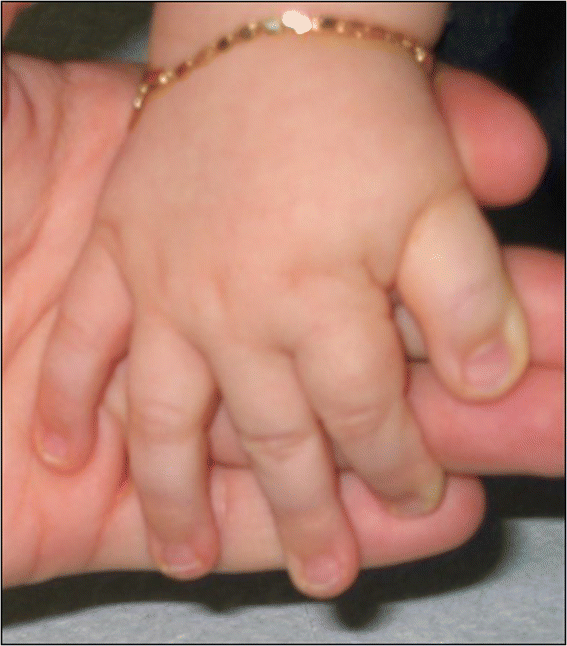
Typical hands of a RSTS patient, including enlarged first finger and clinodactyly of the fifth finger.
Table 1 The incidence of a number of typical features of RSTS
Il periodo neonatale degli individui con RSTS è tipicamente caratterizzato da ipotonia e ritardo nello sviluppo psico-sviluppo motorio, con gradi variabili di disabilità intellettuale. Per esempio, il punteggio del quoziente di intelligenza (QI) dei pazienti con RSTS nel periodo neonatale varia solitamente da 25 a 79 (media: 36-51). Nel 2009, Galèra et al. hanno descritto tre caratteristiche cardinali della RSTS, breve capacità di attenzione, stereotipie motorie e scarsa coordinazione. Sono stati riportati sia pazienti con RSTS classica e lieve disabilità intellettiva che pazienti con RSTS atipica e lieve disabilità intellettiva. Pertanto, nei casi più lievi, una diagnosi precoce è particolarmente difficile, e le principali fasi di sviluppo devono essere rigorosamente seguite per avviare rapidamente una stimolazione specifica e personalizzata. Inoltre, anche se i pazienti RSTS di solito hanno caratteristiche amichevoli e socievoli, i disturbi comportamentali, gli sbalzi d’umore e i disturbi ossessivo-compulsivi possono ancora essere osservati, soprattutto in età adulta.
Transizione e assistenza sanitaria in età adulta
Oltre il 90% degli individui con RSTS sopravvivono fino all’età adulta, e l’assistenza sanitaria per questi pazienti è particolarmente complessa, richiede tempo e spesso non è standardizzata in linee guida specifiche. I problemi medici della maggior parte delle sindromi genetiche spesso cambiano con l’età e c’è una conoscenza limitata sulla gestione degli adulti con sindromi genetiche. Individui adulti con RSTS sono stati documentati, ma solo pochi studi di revisione sugli adulti con RSTS sono disponibili. In questi studi di revisione, i pazienti adulti con RSTS avevano problemi medici rilevanti e la maggior parte di loro aveva sovrappeso o obesità. Un certo numero di fenotipi comportamentali come l’ansia, l’instabilità dell’umore e il comportamento aggressivo possono apparire durante l’adolescenza. I caregiver hanno riportato una diminuzione delle abilità nel tempo nel 32% dei soggetti RSTS e alcuni comportamenti peggiorativi nel 37% dei pazienti RSTS, il che è coerente con il rapporto di Hennekam et al. nel 1992 . Pertanto, la cura di follow-up è importante per identificare e trattare i problemi psichiatrici che emergono con l’età. Infine, la prevalenza della RSTS può essere superiore alla stima originale a causa della diagnosi tardiva, in particolare nei casi più lievi.
Approcci diagnostici
I soggetti con sospetta RSTS dovrebbero essere valutati da genetisti pediatrici esperti in dismorfologia. Un certo numero di tecniche molecolari sono ampiamente utilizzate nelle analisi genetiche della RSTS. Tra i test, l’analisi del cariotipo può mostrare rare anomalie citogeneticamente visibili (traslocazioni, inversioni o delezioni); anche se il risultato è solitamente normale, questa valutazione dovrebbe in ogni caso essere eseguita per identificare possibili riarrangiamenti. La FISH può identificare le microdelezioni, con un tasso di rilevamento del 5-10% . Il test di analisi delle delezioni/duplicazioni identifica delezioni/duplicazioni esoniche o dell’intero gene non rilevabili dall’analisi di sequenza delle regioni codificanti e introniche fiancheggianti del DNA genomico. Possono essere utilizzati vari metodi (PCR quantitativa, PCR a lungo raggio, amplificazione multipla ligation-dependent probe (MLPA) e microarray cromosomico). Stef et al. hanno rilevato delezioni in 17 (20,5%) di 83 pazienti utilizzando l’array-CGH e la PCR quantitativa multiplex a fluorescenza. L’analisi molecolare può anche identificare mutazioni nei geni CREBBP e EP300. Varianti patogene del gene CREBBP sono state identificate nel 50-70% degli individui RSTS, mentre mutazioni nel gene EP300 sono state riportate in circa il 5-8% dei pazienti RSTS da Roelfsema et al. , Bartholdi et al. , Negri et al.
Correlazioni genotipo-fenotipo
Poco si sa sulle correlazioni genotipo-fenotipo della RSTS. Un fenotipo grave è stato riportato nei pazienti RSTS con grandi delezioni, ma altri studi non supportano questa associazione genotipo-fenotipo. Tuttavia, un’associazione tra QI più basso e caratteristiche autistiche con grandi delezioni in pazienti RSTS è possibile. Pertanto, Calì et al. hanno raccomandato MLPA che può identificare queste grandi delezioni per lo screening dei pazienti RSTS con QI inferiore e caratteristiche autistiche. Le mutazioni al di fuori del dominio dell’istone acetiltransferasi (HAT) sono state associate a un fenotipo lieve. Inoltre, il mosaicismo somatico può anche essere associato a RSTS lieve. Meno di 20 pazienti RSTS con mutazioni EP300 sono stati identificati e caratterizzati fino ad ora. Le mutazioni EP300 sono state associate a preeclampsia in donne con una gravidanza affetta da RSTS; sono stati descritti un coinvolgimento cutaneo e un fenotipo lieve con anomalie scheletriche e problemi neuropsichiatrici.
Consulenza genetica
La maggior parte dei casi di RSTS sono sporadici e solo pochi casi di RSTS che colpiscono fratelli e sorelle sono stati riportati finora. La trasmissione verticale è estremamente rara. Mentre il rischio di ricorrenza della RSTS è generalmente basso, una corretta consulenza genetica dovrebbe essere fornita per la diagnosi prenatale della RSTS. Il mosacismo somatico, per esempio, è stato confermato nel padre clinicamente non colpito di un ragazzo con RSTS e nel padre leggermente colpito di tre femmine con RSTS. Inoltre, il mosaicismo germinale è stato ipotizzato in due casi di RSTS. Sulla base di questi rapporti, il rischio di ricorrenza della RSTS è di circa 0,5-1%.
Gestione
Mentre sono stati fatti progressi significativi nella conoscenza delle manifestazioni cliniche e della storia naturale della RSTS, le linee guida per l’assistenza sanitaria e il follow-up della RSTS non sono state ben aggiornate dopo la proposta di Wiley et al. nel 2003 (Tabella 2). Le nuove terapie genetiche ed epigenetiche possono essere approcci promettenti per il trattamento della RSTS, ma c’è un urgente bisogno di migliorare e personalizzare il protocollo standard di follow-up. Sulla base delle nostre conoscenze e degli aspetti critici che discutiamo di seguito, abbiamo redatto la nostra proposta di follow-up (Tabella 3).
La gestione dovrebbe essere adeguata in età adolescenziale, per le differenze note in alcuni aspetti (caratteristiche oftalmologiche, tendenza all’obesità e disturbi dell’umore in particolare).
Sconosciuti e criticità nella RSTS
Sono stati fatti progressi sostanziali negli studi delle basi genetiche e delle problematiche mediche della RSTS, che contribuiscono alla diagnosi clinica iniziale e alla successiva conferma attraverso analisi molecolari. Data la complessità e la rarità di questa sindrome, ci sono ancora numerose domande senza risposta sulla RSTS. Pertanto, ulteriori indagini dovrebbero essere focalizzate sulla diagnosi clinica e la gestione, nonché sulla correlazione genotipo-fenotipo.
Sulla base della nostra esperienza, i modelli di crescita anormale, come si vede sui grafici di crescita standard, dovrebbero essere evidenziati nei criteri diagnostici della RSTS. Inoltre, i criteri diagnostici clinici e lo screening potrebbero essere ulteriormente classificati secondo i periodi prenatale, infantile e adolescenziale. In particolare, la presenza di una crescita normale in utero, associata ad altri marcatori come il pollice largo/alluce e altre malformazioni, è utile nella diagnosi differenziale della RSTS da altre sindromi (per esempio, la sindrome di Cornelia de Lange). I genetisti pediatrici dovrebbero prestare maggiore attenzione alle falangi distali allargate: esaminando le foto dei pazienti inviate alle analisi molecolari abbiamo trovato nella grande maggioranza questo segno, non riportato nelle cartelle cliniche. L’allargamento del primo dito è una caratteristica largamente conosciuta, ma anche comune in altre sindromi come l’acrocefalopolisindattilia, mentre la conformazione delle falangi distali sembra più specifica per la RSTS. Inoltre, le cuspidi dell’artiglio che sono spesso trascurate sono anche altamente specifiche per la RSTS. Uno studio multicentrico di prevalenza delle anomalie cerebrali e della colonna vertebrale è necessario, alla luce delle diverse segnalazioni e del significato sia diagnostico che prognostico di queste caratteristiche; una risonanza magnetica cerebrale/medullare di screening potrebbe essere utile in aggiunta al work-up diagnostico di base. Inoltre, per quanto riguarda le caratteristiche endocrinologiche, sono state recentemente aggiunte ulteriori informazioni, in particolare sulla forma e funzione della tiroide, e siamo personalmente a conoscenza di altri due casi con ipotiroidismo lieve e tiroide piccola. Oltre alla disabilità intellettuale, alcuni cambiamenti comportamentali sono noti per i pazienti RSTS, ma nessuna prova significativa supporta i valori diagnostici di queste caratteristiche neuropsichiatriche nella diagnosi RSTS. Pertanto, nessuna caratteristica neuropsichiatrica è abbastanza forte da essere inclusa nei criteri diagnostici della RSTS anche se alcune caratteristiche possono essere più suggestive di mutazioni EP300. In questi casi, l’ID è lieve o assente, e predomina il disturbo comportamentale (cioè l’ansia). Altre caratteristiche suggestive di mutazioni EP300 includono la pre-eclampsia e anomalie meno significative nella prima cifra, dando lo spunto per la stesura di criteri differenziali per EP300, e per una flow-chart di laboratorio più precisa e individualizzata. Per quanto ne sappiamo, questo è l’unico cambiamento possibile nell’ordine delle indagini molecolari, poiché le altre correlazioni genotipo-fenotipo sono solo provvisorie. Numerose complicazioni non specifiche possono verificarsi durante il follow-up delle RSTS; pertanto, è difficile stabilire un protocollo di follow-up generale ed efficiente. Inoltre, non sono state identificate robuste correlazioni genotipo-fenotipo. In generale, il follow-up ortopedico, il monitoraggio della dieta nell’adolescenza e nei periodi neuropsichiatrici, e le valutazioni oftalmologiche negli adulti dovrebbero essere focalizzate. Un protocollo di follow-up meno rigoroso può essere appropriato solo per i pazienti RSTS con mutazioni EP300, con particolare attenzione ai problemi della pelle (pilomatrixomi e nevi) che sono probabilmente più frequenti che nei pazienti con mutazioni CREBBP. Per quanto riguarda la consulenza genetica, la spazzola salivare e i test genetici sono importanti per la valutazione del rischio di recidiva nei genitori con mosaicismo germinale e somatico.
Una discussione sugli aspetti critici dei progressi nella comprensione dell’eziopatogenesi della RSTS è fuori dallo scopo di questa recensione, ma diversi modelli murini sono stati realizzati con risultati interessanti.

