電解質は、イオンに解離し、それゆえ電荷を輸送することができる化学化合物です – すなわち、電解質は電気伝導体です。
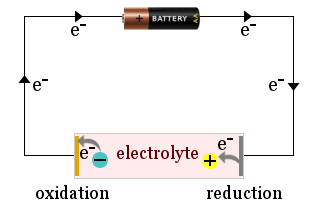
例えば、この図は、家庭用バッテリーを使用して、電解質イオンを電気化学セルの電極に引き寄せ、イオンが電子を獲得 (還元) または電子を失う (酸化) 場合を示しています。
電極自体が反応することもあります。たとえば、金属電極が酸化され、電解質中にイオンを放出することもあります。
電解質は、固体、液体、溶液のいずれでも構いません。
電解質の例
1. 溶融塩化ナトリウムは、ナトリウム金属を製造する際の電解質として働きます。
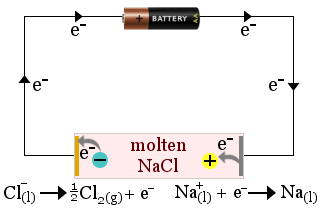
2. 水に溶かした水酸化カリウムにより、初期の充電式細胞であるエディソン細胞で非常に導電性の電解質になっています。
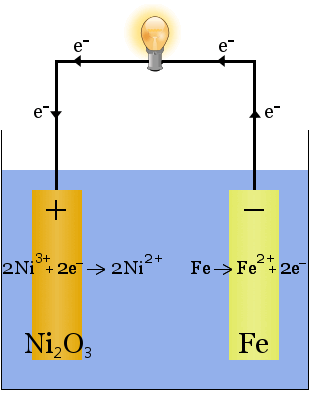
上記のナトリウム生成の場合とは異なり、この反応では電解液は消費されない。この場合の水酸化カリウムの役割は、電解液の伝導率を高め電気回路を完成するために、イオンを増加させることである。
電極での反応の化学式は次のようになります。
放電は左から右、充電は右から左へ式を読んでいくことになる。
3.従来、電解質はイオンが移動できるように液体でしたが、現在はその構造を通してイオンが容易に移動できる固体材料が利用可能です。
リチウム錫リン硫化物Li10SnP2S12は、リチウムイオン電池に使用される固体電解質です。固体電解質の結晶構造とリチウムイオンとの弱い相互作用は、リチウムイオンが容易に通過できる環境を提供します。電解質の主なイオンは、カルシウム(Ca2+)、マグネシウム(Mg2+)、ナトリウム(Na+)、カリウム(K+)、塩化物(Cl-)、炭酸水素(HCO3-)、リン酸水素(HPO42-)であり、これらの電解質は、生体内の電気化学反応に極めて重要な役割を果たしています。
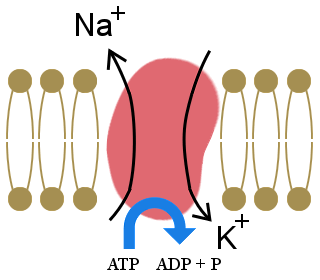
The importance of the sodium-potassium pump, shown in the diagram, to our lives is illustrated by the fact that it uses one-third of our resting energy.The pump maintains our cells’ electrolyte balance, with excess potassium ions inside cells and excess sodium ions outside cells.
This concentration gradient creates a voltage across the cell wall, which allows electrical signals to be transmitted in neurons and in muscles.It also provides the energy for processes in cell-membranes.
