THE ACID-BASE BEHAVIOUR OF AMINO ACIDS
This page looks at what happens to amino acids as you change the pH by adding either acids or alkalis to their solutions.
For simplicity, the page only looks at amino acids which contain a single -NH2 group and a single -COOH group.
Amino acids as zwitterions
Zwitterions in simple amino acid solutions
An amino acid has both a basic amine group and an acidic carboxylic acid group.
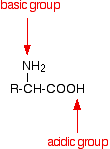
There is an internal transfer of a hydrogen ion from the -COOH group to the -NH2 group to leave an ion with both a negative charge and a positive charge.
This is called a zwitterion.

This is the form that amino acids exist in even in the solid state.
双性イオンとは、全体としては電荷を持たず、プラスとマイナスに分かれている化合物のことです。
アミノ酸溶液へのアルカリ添加
アミノ酸溶液に水酸化物イオンを加えてpHを上げると、-NH3+基から水素イオンが除かれます。
![]()

電気泳動で、アミノ酸がマイナスイオンとして存在することがわかります。
最も単純な電気泳動では、顕微鏡スライドの上に濡らしたろ紙があり、両端にワニ口をつけたバッテリがあるだけでよいのです。
アミノ酸の溶液は無色ですが、ニンヒドリンの溶液をかけると、しばらくしてその位置がわかります。
アミノ酸は陽極(プラス極)に向かって移動することがわかるでしょう。
アミノ酸の溶液に酸を加える
アミノ酸の溶液に酸を加えてpHを下げると、双性イオンの-COO-部分が水素イオンを取り込みます。
![]()
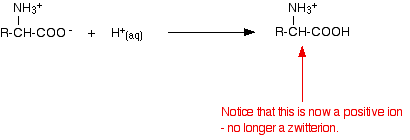
このとき、電気泳動ではアミノ酸は陰極(マイナス極)のほうに移動することになりますね。
pHを極端から極端に変化させる
先ほど酸性で生成したイオンから、徐々にアルカリを加えていくとします。
そのイオンには2つの酸性水素、-COOH基と-NH3+基の水素があります。
このうち酸性が強いのは-COOH基の方なので、まずそれを取り除き、双性イオンに戻します。
![]()
![]()
そこでちょうどよい量のアルカリを加えると、アミノ酸には正負の電荷がなくなり、そのためアミノ酸は、より強い電荷を持つようになります。
この電気泳動中の移動の欠如が起こる pH は、アミノ酸の等電点として知られています。
さらに水酸化物イオンを加えていくと、先ほど見たような、-NH3+基から水素イオンが抜ける反応が起こります。
![]()
![]()
![]()