Typické rysy
Syndrom Rubinstein-Taybi se vyznačuje pomalým vývojem výšky a hmotnosti, mikrocefalií, dysmorfními rysy obličeje, širokými palci a velkými prsty . Prenatální vývoj je normální, s průměrnými nebo téměř normálními růstovými parametry při narození. V prvním postnatálním období se růstové grafy obvykle blíží dolní hranici normálu, což odráží především hypo-krmení zhoršené gastroezofageálním refluxem. Následně lze během dospívání pozorovat tendenci k nadváze nebo obezitě (dříve u mužů než u žen). Pro správné posouzení růstu postižených jedinců jsou nezbytné specifické a nedávno revidované růstové grafy . Rysy obličeje jsou charakterizovány především nízkou frontální vlasovou linií, klenutým/hustým obočím, poklesem palpebrálních štěrbin, odstávajícím zobákovitým nosem s columelou pod alae nasi, dysplastickými a nízko posazenými ušima, klenutým patrem, mírnou mikrognacií, zubními anomáliemi (změněná konstituce, malokluze a převis zubů) a atypickým úsměvem („grimasováním“) s téměř zcela zavřenýma očima (obrázek 1). Na nohou a rukou je typický zvětšený první prst a klinodaktylie pátého prstu (obrázek 2), zatímco polydaktylie s bifidními palci a prvními prsty je pozorována zřídka. Mezi další anomálie skeletu patří abdukované palce, anomálie obratlů, vazivová laxita, těžký a dlouhodobý aseptický zánět hlavice stehenní kosti, anomálie podobné Perthesově chorobě (3 %) a příležitostně sklouznutí kapitálové epifýzy femuru. Zvláště bylo hlášeno vysoké riziko abnormalit krční páteře (nestabilita C1-C2, os odontoideum, hypoplazie dens, fúze krčních obratlů) , s možnou stenózou na kraniovertebrálním přechodu, která může způsobit cervikální myelopatii. Byly hlášeny komplexní neuroradiologické problémy včetně dysgeneze corpus callosum (17 %) , malformace Chiariho typu I se syringomelií nebo bez ní, malformace Dandyho Walkera a hydrocefalu a tethered cord , které jsou stále předmětem zkoumání. Byly rovněž hlášeny cerebrovaskulární abnormality, jako je spontánní disekce supraaortálních tepen a mozkový infarkt v důsledku disekujícího aneuryzmatu přední mozkové tepny . U pacientů s RSTS však může být postižen jakýkoli orgán. Mezi možné malformace, zdravotní problémy a komplikace patří (tabulka 1):
-
vodivá a/nebo senzorineurální hluchota, opakované infekce středního ucha, opakované respirační infekce, imunitní nedostatečnost ;
-
nespecifické abnormality elektroencefalografie (EEG) (57-66 %) a záchvaty (25 %) ;
-
zubní problémy: paznehty (73 %), hypoplazie skloviny a abnormální počet zubů ;
-
vrozené srdeční vady: defekt síňového septa, defekt komorového septa, patentní ductus arteriosus, koarktace aorty, pulmonální stenóza, bikuspidální aortální chlopeň, pseudotruncus, aortální stenóza, dextrokardie, cévní prstence a poruchy vedení (24-38 %) . Příležitostně byla zaznamenána také asociace hypoplastického levého srdce s RSTS ;
-
malformace nadledvin (52 %) a kryptorchismus (78-100 %) ;
-
endokrinní poruchy: vrozená hypotyreóza , hypoplazie štítné žlázy, nedostatek GH a hypofyzární hypoplazie ;
-
gastrointestinální poruchy: gastroezofageální reflux, zácpa (40-74 %) a megakolon/Hirschsprungova choroba ;
-
obstrukční spánková apnoe, anesteziologické a intubační komplikace ;
-
kožní problémy včetně pilomatrixomů, zarostlých nehtů, paronychie a sklonu k tvorbě keloidů (24 %) ;
-
nádorová onemocnění, zejména nervového a vývojového původu (neuroblastom, meduloblastom, oligodendrogliom, meningeom, feochromocytom, rhabdomyosarkom, leiomyosarkom, seminom, odontom, choristom a pilomatrixom . Byly hlášeny také leukémie a lymfomy ;
-
hirsutism
Figure 1 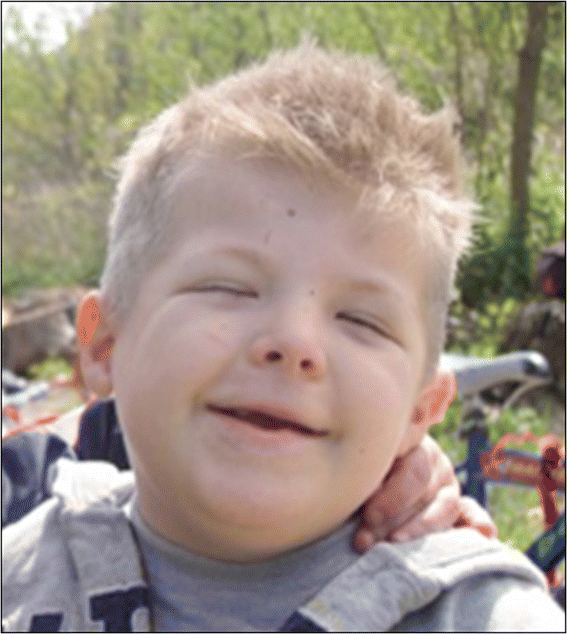
Typical facies of a RSTS patient, including arched eyebrows, slanted palpebral fissures, protruding beaked nose with columella below alae nasi, arched palate, mild micrognathia, labial commissures facing upward, teeth anomalies, and an atypical smile („grimacing“) with nearly completely closed eyes.
Figure 2 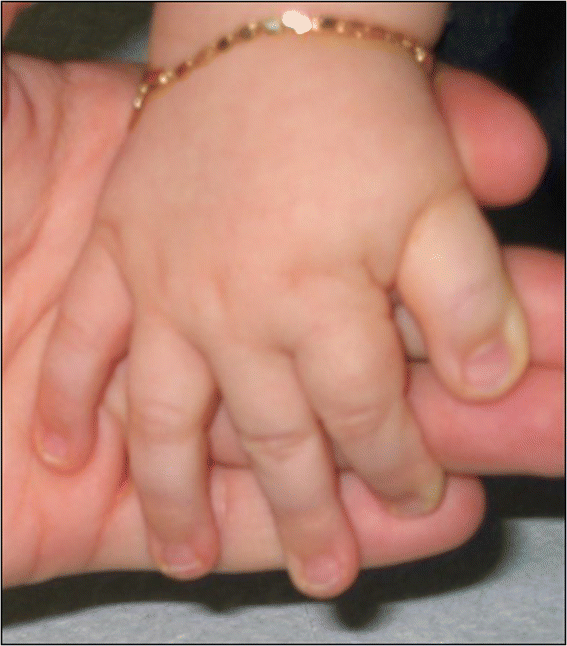
Typical hands of a RSTS patient, including enlarged first finger and clinodactyly of the fifth finger.
Table 1 The incidence of a number of typical features of RSTS
katarakta, jednostranný nebo oboustranný kolobom duhovky/sítnice/optického nervu (9-11 %), glaukom, obstrukce slzných kanálků (38-47 %), refrakční vady (41-56 %) a strabismus (60-71 %) . Kromě toho Jacobs et al. v roce 2012 poprvé popsali periferní avaskulárnost pomocí fluoresceinové angiografie ;
Neonatální období jedinců s RSTS je typicky charakterizováno hypotonií a opožděnou psycho-motorickým vývojem, s různým stupněm mentálního postižení. Například skóre inteligenčního kvocientu (IQ) pacientů s RSTS v novorozeneckém období se obvykle pohybuje v rozmezí 25-79 (průměr: 36-51) . V roce 2009 Galèra a kol. popsali tři kardinální znaky RSTS, a to krátkou dobu pozornosti, motorické stereotypie a špatnou koordinaci . Byli popsáni jak pacienti s klasickou RSTS a lehkým mentálním postižením, tak pacienti s atypickou RSTS a lehkým mentálním postižením . Proto je v nejlehčích případech časná diagnóza obzvláště obtížná a je třeba přísně sledovat hlavní vývojové fáze, aby bylo možné rychle zahájit specifickou a individualizovanou stimulaci. Kromě toho, přestože pacienti s RSTS mají obvykle přátelské a společenské rysy, lze u nich stále pozorovat poruchy chování, výkyvy nálad a obsedantně-kompulzivní poruchy, zejména v dospělosti .
Přechod a zdravotní péče v dospělosti
Více než 90 % jedinců s RSTS se dožije dospělosti , přičemž zdravotní péče o tyto pacienty je obzvláště složitá, časově náročná a často není standardizována v konkrétních pokynech. Zdravotní problémy většiny genetických syndromů se s věkem často mění a znalosti o léčbě dospělých s genetickými syndromy jsou omezené . Dospělí jedinci s RSTS byli zdokumentováni , ale k dispozici je pouze několik přehledových studií o dospělých s RSTS . V těchto přehledových studiích měli dospělí pacienti s RSTS příslušné zdravotní problémy a většina z nich měla nadváhu nebo obezitu. Během dospívání se může objevit řada behaviorálních fenotypů, jako je úzkost, nestabilita nálady a agresivní chování. Pečovatelé uváděli snížení schopností v průběhu času u 32 % osob s RSTS a určité zhoršení chování u 37 % pacientů s RSTS, což je v souladu se zprávou Hennekama a kol. z roku 1992 . Proto je důležitá následná péče pro identifikaci a léčbu psychiatrických problémů, které se objevují s věkem . V neposlední řadě může být prevalence RSTS vyšší než původní odhad v důsledku pozdní diagnózy zejména u mírnějších případů .
Diagnostické přístupy
Jedinci s podezřením na RSTS by měli být vyšetřeni dětskými genetiky znalými dysmorfologie. Při genetických analýzách RSTS se široce používá řada molekulárních technik. Z testů může analýza karyotypu prokázat vzácné cytogeneticky viditelné abnormality (translokace, inverze nebo delece); ačkoli výsledek je obvykle normální, toto hodnocení by mělo být v každém případě provedeno k identifikaci možných přestaveb. Metoda FISH může identifikovat mikrodelece s mírou detekce 5-10 % . Testování deleční/duplikační analýzy identifikuje exonické nebo celogenové delece/duplikace, které nejsou detekovatelné sekvenční analýzou kódujících a doprovodných intronických oblastí genomové DNA. Lze použít různé metody (kvantitativní PCR, PCR s dlouhým dosahem, multiplexní amplifikace sondou závislou na ligaci (MLPA) a chromozomální mikroarray). Stef a kol. zjistili delece u 17 (20,5 %) z 83 pacientů pomocí array-CGH a kvantitativní multiplexní fluorescenční PCR . Molekulární analýzou lze rovněž identifikovat mutace v genech CREBBP a EP300. Patogenní varianty genu CREBBP byly identifikovány u 50-70 % jedinců s RSTS , zatímco mutace v genu EP300 byly Roelfsema et al. , Bartholdi et al. , Negri et al. zaznamenány přibližně u 5-8 % pacientů s RSTS .
Korelace genotypu a fenotypu
O korelacích genotypu a fenotypu u RSTS je známo jen málo. U pacientů s RSTS s velkými delecemi byl zaznamenán závažný fenotyp , ale jiné studie tuto genotypově-fenotypovou asociaci nepotvrzují. Nicméně souvislost mezi nižším IQ a autistickými rysy u pacientů s velkými delecemi RSTS je možná . Calì et al. proto doporučili MLPA, která může tyto velké delece identifikovat pro screening pacientů s RSTS s nižším IQ a autistickými rysy . Mutace mimo doménu histon acetyltransferázy (HAT) byly spojeny s mírným fenotypem . Kromě toho může být s mírnou formou RSTS spojen také somatický mozaicizmus . Doposud bylo identifikováno a charakterizováno méně než 20 pacientů s RSTS s mutacemi EP300 . Mutace EP300 byly spojeny s preeklampsií u žen, které přenášely těhotenství postižené RSTS; bylo popsáno postižení kůže a mírný fenotyp v podobě kosterních abnormalit a neuropsychiatrických problémů .
Genetické poradenství
Většina případů RSTS je sporadická a dosud bylo hlášeno pouze několik případů RSTS postihujících sourozence . Vertikální přenos je extrémně vzácný . Přestože je riziko recidivy RSTS obecně nízké, mělo by být při prenatální diagnostice RSTS poskytnuto řádné genetické poradenství. Somatický mosakismus byl například potvrzen u klinicky nepostiženého otce chlapce s RSTS a u mírně postiženého otce tří žen s RSTS . Kromě toho byla u dvou případů RSTS vyslovena hypotéza o zárodečném mozaicismu . Na základě těchto zpráv je riziko rekurence RSTS přibližně 0,5-1 %.
Management
Přestože došlo k významnému pokroku ve znalostech klinických projevů a přirozeného průběhu RSTS, pokyny pro zdravotní a následnou péči o RSTS nebyly po návrhu Wileyho a kol. v roce 2003 dostatečně aktualizovány (tabulka 2) . Nové genetické a epigenetické terapie mohou být slibnými přístupy k léčbě RSTS , je však naléhavě nutné zlepšit a personalizovat standardní protokol následné péče. Na základě našich poznatků a kritických aspektů, které diskutujeme níže, jsme vypracovali náš návrh následného sledování (tabulka 3).
Management by měl být upraven v adolescentním věku, pro známé rozdíly v některých otázkách (oftalmologické vlastnosti, sklon k obezitě a zejména poruchy nálady).
Neznámé a kritické problémy u RSTS
Významného pokroku bylo dosaženo ve studiu genetického základu a medicínské problematiky RSTS, což přispívá k prvotní klinické diagnostice a následnému potvrzení pomocí molekulárních analýz. Vzhledem ke složitosti a vzácnosti tohoto syndromu však stále existuje řada nezodpovězených otázek týkajících se RSTS. Proto by se další zkoumání mělo zaměřit. na klinickou diagnostiku a léčbu i na korelaci genotypu a fenotypu.
Na základě našich zkušeností by v diagnostických kritériích RSTS měly být zdůrazněny abnormální růstové vzorce, které jsou patrné na standardních růstových grafech. Kromě toho by klinická diagnostická kritéria a screening mohly být dále klasifikovány podle prenatálního, dětského a adolescentního období. Zejména přítomnost normálního růstu in utero spojená s dalšími markery, jako jsou široké palce/halucinace a jiné malformace, je užitečná při diferenciální diagnostice RSTS od jiných syndromů (např. syndrom Cornelia de Lange). Dětští genetici by měli věnovat větší pozornost rozšířeným distálním falangám: při prohlížení fotografií pacientů zaslaných k molekulárním analýzám jsme ve velké většině našli tento znak, který nebyl uveden v klinických kartách. Rozšířený první prst je znak do značné míry známý, ale také běžný u jiných syndromů, jako je akrocefalopolysyndaktylie, zatímco konformace distálních falang se zdá být specifičtější pro RSTS. Kromě toho jsou pro RSTS vysoce specifické i často přehlížené palcové klouby. Vzhledem k několika zprávám a diagnostickému i prognostickému významu těchto znaků je třeba provést multicentrickou studii prevalence abnormalit mozku a páteře; kromě základního diagnostického vyšetření by mohla být užitečná screeningová magnetická rezonance mozku a lebky. Pokud jde o endokrinologické znaky, nedávno přibyly další informace týkající se zejména tvaru a funkce štítné žlázy a osobně víme o dalších dvou případech s mírnou hypotyreózou a malou štítnou žlázou. Kromě intelektuálního postižení jsou u pacientů s RSTS známy některé změny chování, ale žádné významné důkazy nepodporují diagnostickou hodnotu těchto neuropsychiatrických rysů v diagnostice RSTS. Proto nejsou žádné neuropsychiatrické rysy dostatečně silné na to, aby byly zahrnuty do diagnostických kritérií RSTS, i když některé rysy mohou více svědčit pro mutace EP300. V těchto případech je ID mírný nebo chybí a převažují poruchy chování (např. úzkost). Mezi další znaky svědčící pro mutace EP300 patří preeklampsie a méně významné abnormality v prvním čísle, což dává vodítko pro sestavení diferenciálních kritérií pro EP300 a pro přesnější a individualizované laboratorní schéma. Podle našich znalostí je to jediná možná změna v pořadí molekulárních vyšetření, protože ostatní korelace genotyp-fenotyp jsou pouze orientační. Během následné péče o RSTS se mohou vyskytnout četné nespecifické komplikace, proto je obtížné stanovit obecný a účinný protokol následné péče. Kromě toho nebyly zjištěny žádné spolehlivé korelace mezi genotypem a fenotypem. Obecně je třeba se zaměřit na ortopedické sledování, sledování diety v období dospívání a v neuropsychiatrickém období a oftalmologické hodnocení u dospělých. Méně přísný protokol sledování může být vhodný pouze u pacientů s RSTS s mutací EP300 , se zaměřením na kožní problémy (pilomatrixomy a névy), které jsou pravděpodobně častější než u pacientů s mutací CREBBP. Co se týče genetického poradenství, pro vyhodnocení rizika recidivy u rodičů se zárodečným a somatickým mozaicismem jsou důležité slinné kartáčky a genetické testy.
Diskuse o kritických aspektech pokroku v pochopení etiopatogeneze RSTS je mimo rámec tohoto přehledu, ale byly vytvořeny různé myší modely se zajímavými výsledky .

