THE ACID-BASE BEHAVIOUR OF AMINO ACIDS
This page looks at what happens to amino acids as you change the pH by adding either acids or alkalis to their solutions.
For simplicity, the page only looks at amino acids which contain a single -NH2 group and a single -COOH group.
Amino acids as zwitterions
Zwitterions in simple amino acid solutions
An amino acid has both a basic amine group and an acidic carboxylic acid group.
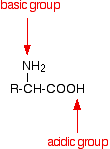
There is an internal transfer of a hydrogen ion from the -COOH group to the -NH2 group to leave an ion with both a negative charge and a positive charge.
This is called a zwitterion.

This is the form that amino acids exist in even in the solid state. Pokud aminokyselinu rozpustíte ve vodě, jednoduchý roztok obsahuje i tento iont.
Zwitterion je sloučenina bez celkového elektrického náboje, která však obsahuje oddělené části, které jsou nabité kladně a záporně.
Přidáním zásady do roztoku aminokyseliny
Zvýšíte-li pH roztoku aminokyseliny přidáním hydroxidových iontů, dojde k odstranění vodíkového iontu ze skupiny -NH3+.
![]()

Pomocí elektroforézy můžete ukázat, že aminokyselina nyní existuje jako záporný iont.
V nejjednodušší podobě může elektroforéza sestávat pouze z kousku navlhčeného filtračního papíru na sklíčku mikroskopu s krokosvorkou na každém konci připojenou k baterii. Do středu papíru se umístí kapka roztoku aminokyseliny.
Ačkoli je roztok aminokyseliny bezbarvý, jeho polohu lze po určité době zjistit postříkáním roztokem ninhydrinu. Pokud se papír nechá zaschnout a poté se mírně zahřeje, aminokyselina se objeví jako barevná skvrna.
Zjistilo by se, že aminokyselina putuje směrem k anodě (kladné elektrodě).
Přidání kyseliny do roztoku aminokyseliny
Snížíte-li pH přidáním kyseliny do roztoku aminokyseliny, část zwitterionu -COO- zachytí vodíkový ion.
![]()
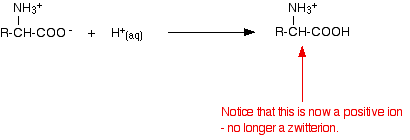
Tentokrát by se při elektroforéze aminokyselina pohybovala směrem ke katodě (záporné elektrodě).
Přesun pH z jednoho extrému do druhého
Předpokládejme, že začneme s iontem, který jsme právě vyrobili za kyselých podmínek, a pomalu k němu přidáváme alkálii.
Tento iont obsahuje dva kyselé vodíky – jeden ve skupině -COOH a jeden ve skupině -NH3+.
Kyselější z nich je ten ve skupině -COOH, a tak se nejprve odstraní ten – a dostanete se zpět ke zwitterionu.
![]()
![]()
Pokud jste tedy přidali správné množství zásady, aminokyselina již nemá čistý kladný ani záporný náboj. To znamená, že by se během elektroforézy nepohybovala ani směrem ke katodě, ani směrem k anodě.
pH, při kterém k tomuto nedostatečnému pohybu během elektroforézy dochází, se nazývá izoelektrický bod aminokyseliny. Toto pH se u jednotlivých aminokyselin liší.
Pokud budete pokračovat v přidávání hydroxidových iontů, dojde k reakci, kterou jsme již viděli a při které se ze skupiny -NH3+ odstraní vodíkový ion.
![]()
![]()