A daratumumab (DARA) egy olyan gyógyszer, amelyet nemrégiben hagyott jóvá az FDA és szabadalmaztatott a Janssen a myeloma multiplex kezelésére. Ez a gyógyszer egy lgG1k CD38-célú monoklonális antitest (MoAb), amely a myelóma-sejtekben expresszálódik; ezekben a betegekben a tumorsejtekre erősen citotoxikus.1-4 A CD38 antigén jelenlétét egészséges egyének eritrocitáinak felszínén is igazolták áramlási citometriával5. Ezenkívül a DARA-val kezelt betegek plazmájában rutinszerű kompatibilitási vizsgálatok során panreaktivitást mutattak ki.6 Ez egy új probléma a transzfúziós medicinában, amely késlelteti a vérkomponensek időben történő szállítását, és így potenciális veszélyt jelent a beteg életére. Mivel a téma nemrégiben jelent meg, a technikai eljárási kézikönyvek (pl. az AABB) nem tartalmaznak specifikus módszertant az ilyen típusú problémák megoldására.
Már több mint 20 éve általánosan használják a ditiotreitol (DDT) redoxi-szerrel kezelt vörösvértesteket a Kell-antigén, valamint más, klinikailag kevésbé jelentős antigéncsoportok denaturálására hemolitikus transzfúziós reakció következtében. Ezt láthatjuk például Landsteiner-Wiener, Cartwright, Dombrock, Indian, Jhon Milton Hagen, Lutheran és Raph esetében. Ez a tulajdonság hasznos az allo-antitestek kutatásában (az AABB technikai kézikönyve).7,8
Újabban bebizonyosodott, hogy a CD38 antigén érzékeny a dithiothreitol (DDT) redoxi szerrel történő denaturálásra is,9 anélkül, hogy a többi klinikailag jelentős eritrocita antigénre hatással lenne. Az interferencia kiküszöbölésének lehetőségei közül a DTT technikát alkalmazzuk, amely lehetővé teszi a klinikailag jelentős antitestek jelenlétének kimutatását, így a beteg számára alacsonyabb transzfúziós kockázatú vérkomponenseket biztosítunk.
Anyagok és módszerek
A Zambrano Hellion kórház vérbankjába 2 egység globuláris csomag és 4 trombocita koncentrátum transzfúziós kérése érkezett. A beteg, egy 64 éves férfi, akinek korábban nem volt transzfúziója, 4 éve fennálló myeloma multiplex diagnózisa volt, és rezisztens volt a hagyományos gyógyszeres kezelésre. A vénás vért EDTA-val vették le. A mintákat a vérbankban alkalmazott hagyományos módszerekkel és technikákkal (pl. mikroagglutinációs technikák gélben) vizsgálták a transzfúzió előtti rutinvizsgálatokra. Az ABO vércsoport és Rh vizsgálatokat Grifols kártyákkal végeztük.
A szabálytalan ellenanyagkövetéshez és azonosításhoz a Grifols teljes Grifols eritrocita panelt, valamint Grifols DG Gel Coombs oszlopokat használtunk. Ezenkívül a transzfúzió előtti kereszthasonlítási teszteket a DG Coombs betétben leírt technika szerint dolgoztuk fel (antihumán globulin poli-specifikus), az eritrociták 0,2M-os, pH 8-as ditiotreitollal (DTT) történő kezelésére, felhasználva a 4. sz.6 módszerét az ABB műszaki kézikönyvének (az általános laboratóriumi módszerek fejezetek 12. kiadása)8 (lásd az 1. ábrát).
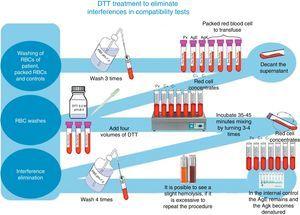 DTT-kezelés az interferenciák kiküszöbölésére a kompatibilitási vizsgálatokban.
DTT-kezelés az interferenciák kiküszöbölésére a kompatibilitási vizsgálatokban.
DTT-kezelés az interferenciák kiküszöbölésére a kompatibilitási tesztekben.
Eredmények
A beteg plazmája pán-reaktivitást mutatott a panel eritrocitáival és ismert antigénekkel, amely homogén módon 3+ intenzitású (0-4. fokozat) reakciómintázatot mutatott (lásd az ábrát.
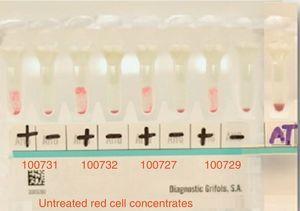
Main cross matching test with 4 donors resulted in incompatibility. Positive=main crossmatching (+), negative=minor crossmatching (−), AT=auto-control crossmatch.
The main cross-matching test resulted in incompatibility with all studied donors (15 in total).
The patient’s erythrocytes presented a negative direct anti-human globulin test (IgG and C3b), as well as a negative control. The presence of hemolysis in the patient’s sample was not detected (see Fig. 3).

Results direct anti-human globulin test (IgG and C3b) presenting negative results.
A beteg plazmájával és a különböző donoroktól származó, korábban DTT-vel kezelt, valamint az ellenanyag-szűrő panelben használt eritrocitákkal végzett vizsgálatok elvégzésekor egyik vizsgált mintában sem találtunk reaktivitást. K+ és E+ kontroll eritrocitákat használtunk annak ellenőrzésére, hogy a DTT csak a K antigént denaturálta, az E antigént pedig megőrizte; ez a vizsgálatunk minőségellenőrzésének része volt annak megállapítására, hogy a klinikailag jelentős antitestekkel kapcsolatos egyéb antigének inaktívak-e (lásd a 4. ábrát).

Az antitest-szűrő panel eritrociták DTT-triátruma, amely 4 véradó esetében negatív eredményt mutat. C1 (kontroll pozitív) C2 (kontroll negatív).
Diszkusszió
Az anti-CD38 alkalmazása ígéretes kezelés a myeloma multiplexben szenvedő betegek számára, és jelenleg más típusú rosszindulatú daganatok esetében is vizsgálják. A probléma az, hogy ez a gyógyszer megzavarja a kompatibilitási teszteket, így megnehezíti a vérkomponensek időben történő és biztonságos szállítását.
Bizonyítékok vannak arra, hogy a DARA-val kezelt betegek szérumában lévő anti-CD38 kötődik az antitestkövető panelben használt eritrocitákban, valamint a transzfúzió előtti keresztillesztési teszt donorjaiban kifejeződő CD38 antigénhez, pán-reaktivitást generálva. Ez elfedheti a klinikailag jelentős antitestek jelenlétét, különösen többszülős betegeknél vagy poli-transzfundált betegeknél. Ez a pán-reaktivitás semlegesítő szerek alkalmazásával visszafordítható, amelyek helyreállítják a szabálytalan antitest-azonosítást és a követési teszteket. Az antiidiotípusos antitesteket, valamint a szolubilis rekombináns CD38-at korábbi cikkekben pozitív eredményekkel értékelték.
A vérbankban rendelkezésre álló lehetőségek közül, hogy ezt az interferenciát kiküszöböljük, a DDT technikát alkalmaztuk. Ennek legjobb tulajdonsága, hogy egy redox-szer, amely a fehérje tercier szerkezetét szakítja meg azáltal, hogy a diszulfidkötéseket irreverzibilisen szabad szulfhidrillé redukálja. A tercier szerkezet nélkül a fehérjét tartalmazó antigének nem képesek többé antitesteket megkötni, így gátolják a szerológiai reaktivitást. Ennek a technikának az a potenciális problémája, hogy más vércsoport-antigéneket is érint. A mindennapi gyakorlatban azonban csak a K antigénnek van klinikai jelentősége. Ezért a DARA-val kezelt betegeknek csak K-erythrocitakoncentrátummal ajánlott transzfundálni. Lehetőség van arra is, hogy más ágensekkel, például K és Yta reagálókkal szemben is elveszíthetik a reaktivitásukat. Mindazonáltal ez rendkívül ritka eseménynek bizonyul. A DDT nem inaktiválja a legtöbb klinikailag jelentős és gyakori antigén, mint például az Rh, Duffy, Kidd és MNS rendszerek szerológiai aktivitását. Bölcs dolog a DARA kezelés megkezdése előtt meghatározni a beteg fenotípusát vagy genotípusát.
Az immunhámológiában aggodalomra ad okot az ilyen típusú interferencia lehetséges növekedése a rutin vérátömlesztési vizsgálatokban, amely a rákos betegeknél alkalmazott új monoklonális antitest terápiák következményeként jelentkezhet.
Végeredményben tanulmányunk azt mutatta, hogy az eritrociták DTT-vel történő kezelése inaktiválja a CD38 antigént, megszüntetve a DARA-val kezelt beteg szérumával való reaktivitást. Ez az egyszerű és praktikus módszer lehetővé teszi a vizsgálatok elvégzését anélkül az interferencia nélkül, amelyet az alloantitestek jelenléte okozhat az ezen monoklonális ellenanyagon alapuló terápiában részesülő betegek transzfúziós reakcióiban.
A pánreaktivitás problémája, amely interferenciát okoz a DARA-val kezelt betegek kompatibilitási vizsgálataiban, technikailag megoldható a potenciális véradókból származó eritrociták DTT-vel történő kezelésével. Ez a szer inaktiválja az ezekben a sejtekben jelen lévő CD38 antigént. Ez a panreaktivitás nem késleltetheti a vérkészítmények szállítását, amelyek vészhelyzetben a vérbank gyakorlatának megfelelően azonos ABO globuláris csomagokat és Rh-kompatibilis vörösvértesteket használnak. Ez szükségessé teszi ajánlások és/vagy útmutatók kidolgozását a kezelőorvosok és az ilyen típusú betegeket ellátó vérbankok személyzete számára. Fontos figyelembe venni, hogy a mai napig nem figyeltek meg hemolitikus transzfúziós reakciókat a DARA-val kezelt mintegy 2000 betegnél.8 A DARA-val kezelt betegek transzfúziós biztonságára vonatkozó, mintegy 76 000 gyógyszeralkalmazási ciklust magában foglaló legújabb kutatások nem találtak egyetlen transzfúziós hemolízisre utaló mellékhatást sem.10-12
Az onkohematológus és a vérbank közös munkájának már a betegek kórházi felvételétől kezdve jelen kell lennie. Az ilyen típusú betegeknél alkalmazott transzfúziós eljárásoknak tartalmazniuk kell a teljes eritrocita fenotípus azonosítását a dobozból a vércsoportjával együtt, és a kompatibilitási teszteket a legjobb tudásunk szerint el kell végezni a gyógyszer alkalmazása előtt.
A fent leírt DTT deaktiválási technika minden esetben a transzfúzió biztonságának alternatív mércéjét jelenti. Vérbankunk hazánkban úttörőnek számít e nemrégiben leírt és nemzetközileg validált technológia alkalmazásában.13 Kritikus transzfúziós vészhelyzetekben azonban, amikor a beteg élete veszélyben van, csak ABO és RhD kompatibilitással rendelkező vért szabad transzfundálni, a kompatibilitási tesztek elvégzése nélkül, a sürgősségi transzfúzióknál korábban leírt irányelvek és eljárások szerint.
Erdélyi összeférhetetlenség
A szerzőknek nincs bejelenteni való érdekellentétük.
A szerzőknek nincs bejelenteni való érdekellentétük.