Daratumumab (DARA) è un farmaco recentemente approvato dalla FDA e brevettato dalla Janssen per il trattamento del mieloma multiplo. Questo farmaco è un anticorpo monoclonale (MoAb) lgG1k CD38-targeted che è espresso nelle cellule di mieloma; è altamente citotossico per le cellule tumorali in questi pazienti.1-4 La presenza dell’antigene CD38 sulla superficie degli eritrociti di individui sani è stata dimostrata anche dalla citometria a flusso.5 Inoltre, la panreattività è stata rilevata nel plasma di pazienti trattati con DARA nei test di compatibilità di routine.6 Questo è un nuovo problema nella medicina trasfusionale che ritarda la consegna tempestiva dei componenti del sangue, rappresentando così un potenziale pericolo per la vita del paziente. Essendo un argomento di recente comparsa, i manuali di procedura tecnica (cioè l’AABB), non contemplano una metodologia specifica per la risoluzione di questo tipo di problemi.
Da oltre 20 anni, il trattamento dei globuli rossi con l’agente redox ditiotreitolo (DDT) è stato comunemente usato per denaturare l’antigene Kell, così come altri gruppi di antigeni meno clinicamente significativi come risultato di una reazione emolitica trasfusionale. Possiamo vedere questo come nei casi di Landsteiner-Wiener, Cartwright, Dombrock, Indian, Jhon Milton Hagen, Lutero e Raph. Questa caratteristica è utile nella ricerca degli allo-anticorpi (manuale tecnico dell’AABB).7,8
Più recentemente è stato dimostrato che l’antigene CD38 è anche sensibile alla denaturazione mediante l’agente redox ditiotreitolo (DDT),9 senza che ciò influenzi il resto degli antigeni eritrocitari clinicamente significativi. Tra le possibilità di eliminare l’interferenza, applichiamo la tecnica del DDT, che ci permette di rilevare la presenza di anticorpi clinicamente significativi, fornendo così emocomponenti con un minor rischio trasfusionale per il paziente.
Materiali e metodi
La banca del sangue dell’ospedale Zambrano Hellion ha ricevuto una richiesta di trasfusione di 2 unità di pacchetti globulari e 4 concentrati piastrinici. Il paziente, un uomo di 64 anni senza trasfusioni nel suo passato, aveva una diagnosi di mieloma multiplo con un’evoluzione di 4 anni ed era resistente al trattamento medico convenzionale. Il sangue venoso è stato raccolto con EDTA. I campioni sono stati studiati per i test pre-trasfusionali di routine attraverso i metodi e le tecniche convenzionali utilizzati nella banca del sangue (cioè, tecniche di micro-agglutinazione in gel). Gli studi sul gruppo sanguigno ABO e Rh sono stati eseguiti con le carte Grifols.
Per il monitoraggio e l’identificazione degli anticorpi irregolari, abbiamo utilizzato un pannello completo di eritrociti Grifols, così come le colonne Grifols DG Gel Coombs. Inoltre, i test di cross-matching pre-trasfusione sono stati elaborati secondo la tecnica descritta nell’inserto DG Coombs (anti globulina umana polispecifica), per il trattamento degli eritrociti con ditiotreitolo (DTT) a 0,2M, pH 8, utilizzando il 4.6 del manuale tecnico dell’ABB (12° edizione delle sezioni sui metodi generali di laboratorio)8 (vedi Fig. 1).
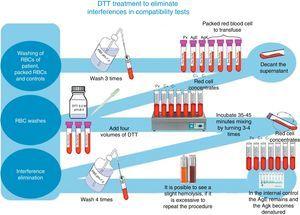
Trattamento con DTT per eliminare le interferenze nei test di compatibilità.
Risultati
Il plasma del paziente ha presentato pan-reattività con gli eritrociti del pannello e antigeni noti, che hanno mostrato un pattern di reazione con intensità 3+ (grado 0-4) in modo omogeneo (vedi Fig. 2).
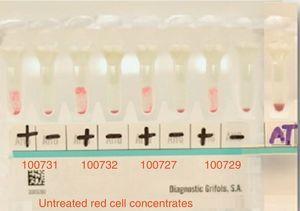
Main cross matching test with 4 donors resulted in incompatibility. Positive=main crossmatching (+), negative=minor crossmatching (−), AT=auto-control crossmatch.
The main cross-matching test resulted in incompatibility with all studied donors (15 in total).
The patient’s erythrocytes presented a negative direct anti-human globulin test (IgG and C3b), as well as a negative control. The presence of hemolysis in the patient’s sample was not detected (see Fig. 3).

Results direct anti-human globulin test (IgG and C3b) presenting negative results.
Al momento di condurre i test con il plasma del paziente e gli eritrociti precedentemente trattati con DTT dai diversi donatori, così come quelli utilizzati nel pannello di screening anticorpale, non abbiamo trovato reattività in nessuno dei campioni studiati. Gli eritrociti di controllo K+ ed E+ sono stati utilizzati per verificare che il DTT denaturasse solo l’antigene K e conservasse l’antigene E; questo faceva parte del controllo di qualità del nostro studio per determinare che altri antigeni relativi ad anticorpi clinicamente significativi fossero inattivi (vedi Fig. 4).
 Gli eritrociti del pannello di screening anticorpale DTT threated, mostrando risultati negativi in 4 donatori di sangue. C1 (controllo positivo) C2 (controllo negativo).
Gli eritrociti del pannello di screening anticorpale DTT threated, mostrando risultati negativi in 4 donatori di sangue. C1 (controllo positivo) C2 (controllo negativo).Pannello di screening anticorpale eritrociti DTT threated, mostrando risultati negativi in 4 donatori di sangue. C1 (controllo positivo) C2 (controllo negativo).
Discussione
L’uso di anti-CD38 è un trattamento promettente per i pazienti con mieloma multiplo ed è attualmente in studio per altri tipi di neoplasie maligne. Il problema è che questo farmaco interferisce con i test di compatibilità, complicando così la consegna tempestiva e sicura dei componenti del sangue.
C’è l’evidenza che gli anti-CD38 nel siero dei pazienti trattati con DARA si legano con l’antigene CD38 espresso negli eritrociti utilizzati nel pannello di tracciamento degli anticorpi, così come nei donatori del test di cross-matching pre-trasfusione, generando una pan-reattività. Questo può mascherare la presenza di anticorpi clinicamente significativi, specialmente in pazienti pluripare o in pazienti politrasfusi. Questa pan-reattività può essere invertita attraverso l’uso di agenti neutralizzanti, che ristabiliscono l’identificazione degli anticorpi irregolari e i test di tracciamento. Gli anticorpi anti-idiotipi, così come il CD38 ricombinante solubile, sono stati valutati in articoli precedenti con risultati positivi.
Tra le possibilità disponibili per eliminare questa interferenza nella banca del sangue, abbiamo utilizzato la tecnica DDT. La sua caratteristica migliore è il fatto che si tratta di un agente redox che interrompe la struttura terziaria della proteina riducendo irreversibilmente i legami disolfuro a solfidrilici liberi. Senza una struttura terziaria, gli antigeni, che contengono proteine, non possono più fissare gli anticorpi, inibendo così la reattività sierologica. Un potenziale problema con questa tecnica è che colpisce anche altri antigeni del gruppo sanguigno. Tuttavia, nella pratica quotidiana, è solo l’antigene K che è clinicamente significativo. Pertanto, si raccomanda ai pazienti trattati con DARA di essere trasfusi solo con concentrati eritrocitari K. Esiste anche la possibilità di perdere la reattività ad altri agenti come K e Yta. Tuttavia, questo risulta essere un evento estremamente raro. Il DDT non disattiva l’attività sierologica della maggior parte degli antigeni clinicamente significativi e frequenti come i sistemi Rh, Duffy, Kidd e MNS. È saggio determinare il fenotipo o il genotipo del paziente prima di iniziare il trattamento con DARA.
In Immunoematologia, c’è preoccupazione per il possibile aumento di questo tipo di interferenza nei test trasfusionali di routine, che può sorgere come conseguenza delle nuove terapie con anticorpi monoclonali nei pazienti con cancro.
In conclusione, il nostro studio ha dimostrato che il trattamento degli eritrociti con DTT inattiva l’antigene CD38, eliminando la reattività con il siero del paziente trattato con DARA. Questo metodo semplice e pratico permette di eseguire studi senza l’interferenza che la presenza di alloanticorpi può causare nelle reazioni trasfusionali nei pazienti che ricevono una terapia a base di questo anticorpo monoclonale.
Il problema della panreattività che causa interferenze nei test di compatibilità dei pazienti trattati con DARA può essere tecnicamente risolto con il trattamento degli eritrociti con DTT da potenziali donatori di sangue. Questo agente disattiva l’antigene CD38 presente in queste cellule. Questa panreattività non dovrebbe ritardare la consegna degli emoderivati, che in situazioni di emergenza saranno utilizzando pacchetti globulari ABO identici e globuli rossi compatibili Rh, secondo le pratiche della banca del sangue. Questo, obbliga a generare raccomandazioni e/o guide per i medici curanti e il personale delle banche del sangue che si occupano di questi tipi di pazienti. È importante considerare che, ad oggi, non sono state osservate reazioni trasfusionali emolitiche nei circa 2000 pazienti trattati con DARA.8 Una recente ricerca sulla sicurezza trasfusionale in pazienti trattati con DARA, comprendente circa 76.000 cicli di applicazione del farmaco, non ha riscontrato una sola reazione avversa all’emolisi trasfusionale.10-12
Il lavoro congiunto dell’onco-ematologo e della banca del sangue deve essere presente fin dal momento dell’ammissione dei pazienti in ospedale. Le procedure di trasfusione applicate a questi tipi di pazienti devono includere l’identificazione del fenotipo eritrocitario completo dalla scatola con il suo gruppo sanguigno, e i test di compatibilità devono essere eseguiti al meglio delle nostre possibilità prima dell’applicazione di questo farmaco.
La tecnica di disattivazione del DTT descritta sopra rappresenta una misura alternativa di sicurezza trasfusionale in tutti i casi. La nostra banca del sangue è un pioniere nel nostro paese nell’adozione di questa tecnologia recentemente descritta e convalidata a livello internazionale.13 Tuttavia, in situazioni critiche di emergenza trasfusionale dove la vita del paziente è in pericolo, il sangue dovrebbe essere trasfuso solo con compatibilità ABO e RhD, senza eseguire i test di compatibilità secondo le politiche e le procedure precedentemente descritte nelle trasfusioni di emergenza.
Conflitto di interesse
Gli autori non hanno conflitti di interesse da dichiarare.