ダラツムマブ(DARA)は、最近FDAによって承認され、ヤンセン社が多発性骨髄腫の治療薬として特許を取得している薬です。 この薬剤は、骨髄腫細胞に発現するlgG1k CD38標的モノクローナル抗体(MoAb)であり、これらの患者の腫瘍細胞に対して高い細胞毒性を示す。1-4 健康体の赤血球の表面にCD38抗原が存在することは、フローサイトメトリーでも証明されている5。 さらに、DARAで治療された患者の血漿には、ルーチンの適合性試験で汎反応性が検出されています。6 これは、輸血医療における新たな問題で、血液成分の適時供給を遅らせ、患者の生命を危険にさらす可能性があります。
20年以上にわたって、酸化還元剤ジチオスレイトール (DDT) による赤血球処理は、溶血性輸血反応の結果として、ケル抗原および臨床的に重要でない他の抗原群を変性させるために一般的に使用されてきました。 Landsteiner-Wiener、Cartwright、Dombrock、Indian、Jhon Milton Hagen、Lutheran、Raphの例のように見ることができる。 この特徴は、同種抗体の研究に有用です(AABBの技術マニュアル)7,8
最近では、CD38抗原は、臨床的に重要な他の赤血球抗原に影響を与えることなく、酸化還元剤ジチオスレイトール(DDT)9による変性にも敏感であることが証明されています。 干渉を根絶する可能性の中で、我々は臨床的に重要な抗体の存在を検出することができるDTT技術を適用し、その結果、患者にとって輸血リスクの低い血液成分を提供します。
材料と方法
Zambrano Hellion病院の血液バンクは、2単位の球状パッケージと4単位の血小板濃縮物の輸血要請を受け取りました。 患者は64歳男性で,これまでの経歴に輸血歴はなく,4年経過した多発性骨髄腫と診断され,従来の内科的治療には抵抗があった。 静脈血はEDTAで採取された。 このサンプルは、血液銀行で使用されている従来の方法と技術(すなわち、ゲルでの微量凝集法)により、ルーチンの輸血前検査のために調査された。 ABO血液型検査とRhはGrifolsカードで行われました。
不規則な抗体の追跡と同定のために、完全なGrifols赤血球パネルとGrifols DG Gel Coombsカラムが使用されました。 さらに、輸血前クロスマッチングテストは、DG Coombs挿入物(抗ヒトグロブリンポリ特異的)に記載されている技術に従って処理され、0.2M、pH 8のジチオスレイトール(DTT)による赤血球の処理について、4.を利用しました。
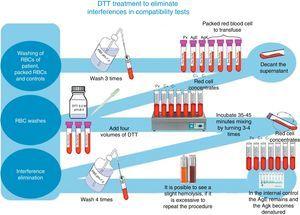
適合性試験の干渉を排除するためのDTT処理
結果
患者の血漿はパネル赤血球および既知の抗原との汎反応性を示し、3+強度(グレード0-4)で均一に反応パターンが見られた(図1参照)。
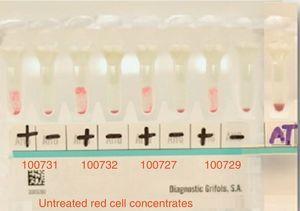
Main cross matching test with 4 donors resulted in incompatibility. Positive=main crossmatching (+), negative=minor crossmatching (−), AT=auto-control crossmatch.
The main cross-matching test resulted in incompatibility with all studied donors (15 in total).
The patient’s erythrocytes presented a negative direct anti-human globulin test (IgG and C3b), as well as a negative control. The presence of hemolysis in the patient’s sample was not detected (see Fig. 3).

Results direct anti-human globulin test (IgG and C3b) presenting negative results.
患者の血漿と、異なるドナーのDTTで事前に処理した赤血球、および抗体スクリーニングパネルで使用した赤血球で試験を行った時点では、研究サンプルのいずれでも反応性を見つけることはありませんでした。 K+およびE+対照赤血球は、DTTがK抗原のみを変性させ、E抗原を保存することを確認するために使用されました。これは、臨床的に重要な抗体に関連する他の抗原が不活性であることを確認するための研究の品質管理の一部でした(図4参照)

。
抗体スクリーニングパネル赤血球DTTスレッド、4人の血液ドナーで負の結果を示した。 C1(コントロール陽性)C2(コントロール陰性).
議論
抗CD38の使用は、複数の骨髄腫の患者に対する有望な治療法で、現在他の種類の悪性新生物に対しても研究中である。
DARAで治療した患者の血清中の抗CD38は、抗体追跡パネルで利用される赤血球に発現するCD38抗原と、輸血前のクロスマッチングテストのドナーに結合し、汎反応を生成するという証拠がある。 これは、特に多胎児患者や多血輸血患者において、臨床的に重要な抗体の存在を覆い隠してしまう可能性があります。 この汎反応は、中和剤の使用により逆転させることができ、不規則な抗体の同定および追跡検査を再確立することができます。
血液バンクにおけるこの干渉を除去するために利用可能な方法のうち、私たちは DDT 技術を使用しました。 その最大の特徴は、ジスルフィド結合を遊離のスルフヒドリルに不可逆的に還元することによって、タンパク質の三次構造を中断させる酸化還元剤であるという事実である。 三次構造がなければ、タンパク質を含む抗原は抗体を固定することができなくなり、血清反応性が阻害される。 この手法の問題点は、他の血液型抗原にも影響を与えることである。 しかし、日常の診療では、臨床的に重要なのはK抗原だけである。 したがって、DARAによる治療を受けた患者には、K-赤血球濃縮液のみを輸血することが推奨されます。 KやYtaのような他の薬剤に対する反応性を失う可能性も存在します。 しかし、これは極めて稀な事象であることが判明しています。 DDTは、Rh、Duffy、Kidd、MNS系など、臨床的に重要で頻度の高いほとんどの抗原の血清活性を失活させるものではありません。
免疫血液学では、がん患者における新しいモノクローナル抗体療法の結果として生じる可能性のある、ルーチンの輸血検査におけるこの種の干渉の増加が懸念されています。
結論として、私たちの研究は、DTTによる赤血球の処理がCD38抗原を不活性化し、DARAで治療した患者の血清との反応性を排除していることを実証しました。
DARAで治療した患者の適合性テストに干渉を引き起こす汎反応性の問題は、潜在的な献血者の赤血球をDTTで処理することで技術的に解決することが可能です。 この薬剤は、これらの細胞に存在するCD38抗原を不活性化させます。 この汎反応性は、緊急事態において、血液銀行の実務に従って、同一のABO球形分包とRh適合赤血球を使用する血液製剤の納入を遅らせてはならない。 このため、この種の患者を担当する血液銀行の医師やスタッフに対する勧告やガイドを作成する必要があります。 8 約76,000サイクルの薬剤適用からなるDARAによる治療を受けた患者の輸血安全性に関する最近の研究では、輸血溶血の有害反応は1件も見つかっていません。10-12
腫瘍血液学者と血液銀行の共同作業は、患者が入院した瞬間から存在しなければなりません。 これらのタイプの患者に適用される輸血の手順には、その血液型と箱から完全な赤血球の表現型を識別することが含まれるべきで、この薬の適用前に適合性テストを可能な限り実行しなければなりません。
上記のDTT不活性化技術は、すべてのケースで輸血の安全性の代替策となるものです。 しかし、患者の生命が危険にさらされている輸血の緊急事態では、以前に緊急輸血で説明した方針と手順に従って適合性試験を行わず、ABOとRhDの適合性のある血液のみを輸血すべきです。
利益相反
著者は申告すべき利益相反はありません
。