Typowe cechy
Zespół Rubinsteina-Taybiego charakteryzuje się powolnym rozwojem wzrostu i masy ciała, mikrocefalią, dysmorficznymi rysami twarzy, szerokimi kciukami i dużymi palcami u stóp. Rozwój prenatalny jest prawidłowy, z przeciętnymi lub prawie normalnymi parametrami wzrostu po urodzeniu. W pierwszym okresie postnatalnym wykresy wzrostu zbliżają się do dolnej granicy normy, co odzwierciedla przede wszystkim niedokarmianie nasilone przez refluks żołądkowo-przełykowy. Następnie w okresie dojrzewania można zaobserwować tendencję do nadwagi lub otyłości (wcześniej u mężczyzn niż u kobiet). Do prawidłowej oceny wzrostu chorych niezbędne są aktualne i aktualne tabele wzrostu. Rysy twarzy charakteryzują się przede wszystkim niską linią czołową włosów, łukowatymi/grubymi brwiami, przesunięciem ku dołowi bruzd powiekowych, wystającym dziobatym nosem z kolumną poniżej łuku brwiowego, dysplastycznymi i nisko osadzonymi uszami, łukowatym podniebieniem, łagodną mikrognatią, anomaliami stomatologicznymi (zmieniony pokrój, wady zgryzu i stłoczenie zębów) oraz nietypowym uśmiechem („grymasem”) z prawie całkowicie zamkniętymi oczami (ryc. 1). W obrębie stóp i dłoni typowe jest powiększenie pierwszego palca i klinodaktylia piątego palca (ryc. 2), natomiast rzadko obserwuje się polidaktylię z dwupalczastymi kciukami i pierwszymi palcami. Do innych anomalii szkieletowych należą: koślawe kciuki, anomalie kręgów, wiotkość więzadeł, ciężkie i długotrwałe aseptyczne zapalenie głowy kości udowej, anomalie podobne do choroby Perthesa (3%) oraz sporadycznie ześlizgnięcie się nasady kości udowej. Szczególnie duże jest ryzyko wystąpienia nieprawidłowości w obrębie kręgów szyjnych (niestabilność C1-C2, os odontoideum, hipoplazja densa, fuzja kręgów szyjnych), z możliwością zwężenia połączenia czaszkowo-kręgowego, co może być przyczyną mielopatii szyjnej. Złożone problemy neuroradiologiczne, w tym dysgenezja ciała modzelowatego (17%), malformacja Chiariego typu I z lub bez syringomielii, malformacja Dandy’ego Walkera i wodogłowie oraz skrępowany rdzeń zostały zgłoszone i są nadal badane. Zgłaszano również nieprawidłowości w układzie naczyniowo-mózgowym, takie jak samoistne rozwarstwienie tętnic nadaortalnych i zawał mózgu spowodowany tętniakiem rozwarstwiającym tętnicy przedniej mózgu. Jednakże u pacjentów z RSTS każdy narząd może być dotknięty chorobą. Możliwe wady rozwojowe, problemy medyczne i powikłania obejmują (Tabela 1):
-
głuchotę przewodzeniową i/lub odbiorczą, nawracające infekcje ucha środkowego, nawracające infekcje układu oddechowego, niedobory odporności ;
-
niespecyficzne nieprawidłowości elektroencefalografii (EEG) (57-66%) i napady drgawkowe (25%) ;
-
katarakta, jednostronna lub obustronna koloboma tęczówki/siatkówki/nerwu wzrokowego (9-11%), jaskra, niedrożność przewodu łzowego (38-47%), wady refrakcji (41-56%) i zez (60-71%) . Ponadto, Jacobs i wsp. po raz pierwszy opisali awaskularyzację obwodową za pomocą angiografii fluoresceinowej w 2012 roku ;
-
Problemy stomatologiczne: kłykcie talonów (73%), hipoplazja szkliwa i nieprawidłowa liczba zębów ;
-
wrodzone choroby serca: ubytek przegrody międzyprzedsionkowej, ubytek przegrody międzykomorowej, drożny przewód tętniczy, koarktacja aorty, zwężenie tętnicy płucnej, dwupłatkowa zastawka aortalna, pseudotruncus, zwężenie aorty, dekstrokardia, pierścienie naczyniowe, zaburzenia przewodzenia (24-38%).
-
Wady rozwojowe nadnerczy (52%) i wnętrostwo (78-100%) ;
-
Zaburzenia endokrynologiczne: wrodzona niedoczynność tarczycy, hipoplazja tarczycy, niedobór GH i hipoplazja przysadki ;
-
Zaburzenia żołądkowo-jelitowe: refluks żołądkowo-przełykowy, zaparcia (40-74%), choroba megacolon/Hirschsprunga ;
-
obturacyjny bezdech senny, powikłania znieczulenia i intubacji ;
-
problemy skórne, w tym pilomatrixomy, wrastające paznokcie, paronychia, skłonność do tworzenia keloidów (24%);
-
nowotwory, szczególnie pochodzenia nerwowego i rozwojowego (neuroblastoma, medulloblastoma, oligodendroglioma, meningeoma, pheochromocytoma, rhabdomyosarcoma, leiomyosarcoma, seminoma, odontoma, choristoma i pilomatrixoma . Zgłaszano również występowanie białaczki i chłoniaka;
-
hirsutism
Figure 1 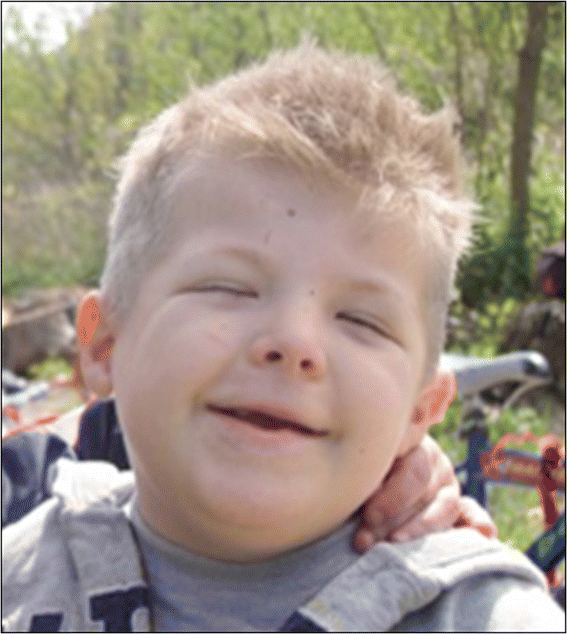
Typical facies of a RSTS patient, including arched eyebrows, slanted palpebral fissures, protruding beaked nose with columella below alae nasi, arched palate, mild micrognathia, labial commissures facing upward, teeth anomalies, and an atypical smile („grimacing”) with nearly completely closed eyes.
Figure 2 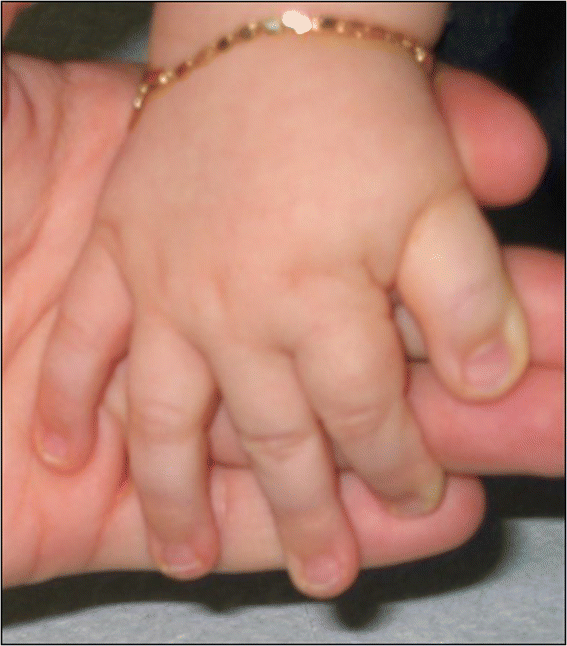
Typical hands of a RSTS patient, including enlarged first finger and clinodactyly of the fifth finger.
Table 1 The incidence of a number of typical features of RSTS
Okres noworodkowy osób z RSTS charakteryzuje się zwykle hipotonią i opóźnionym rozwojem psycho-rozwój psycho-ruchowy, z różnym stopniem niepełnosprawności intelektualnej. Na przykład, wynik ilorazu inteligencji (IQ) pacjentów z RSTS w okresie noworodkowym zwykle waha się od 25 do 79 (średnio: 36-51). W 2009 roku Galèra i wsp. opisali trzy charakterystyczne cechy RSTS: krótki czas koncentracji uwagi, stereotypie ruchowe i słaba koordynacja. Zgłaszano zarówno pacjentów z klasycznym RSTS i lekką niepełnosprawnością intelektualną, jak i pacjentów z atypowym RSTS i lekką niepełnosprawnością intelektualną. Dlatego też, w najłagodniejszych przypadkach, wczesna diagnoza jest szczególnie trudna, a główne etapy rozwoju muszą być ściśle monitorowane w celu szybkiego rozpoczęcia specyficznej i zindywidualizowanej stymulacji. Ponadto, chociaż pacjenci z RSTS zazwyczaj mają przyjazne i towarzyskie cechy, nadal można zaobserwować zaburzenia zachowania, wahania nastroju i zaburzenia obsesyjno-kompulsywne, szczególnie w wieku dorosłym.
Przejście i opieka zdrowotna w wieku dorosłym
Ponad 90% osób z RSTS przeżywa do wieku dorosłego, a opieka zdrowotna dla tych pacjentów jest szczególnie złożona, czasochłonna i często nie jest ustandaryzowana w konkretnych wytycznych. Problemy medyczne związane z większością zespołów genetycznych często zmieniają się wraz z wiekiem, a wiedza na temat postępowania u dorosłych z zespołami genetycznymi jest ograniczona. Udokumentowano występowanie RSTS u osób dorosłych, ale dostępnych jest tylko kilka badań przeglądowych dotyczących osób dorosłych z RSTS. W tych badaniach przeglądowych, dorośli pacjenci z RSTS mieli istotne problemy medyczne, a większość z nich miała nadwagę lub otyłość. Szereg fenotypów behawioralnych, takich jak lęk, niestabilność nastroju i zachowania agresywne, może pojawić się w okresie dojrzewania. Opiekunowie zgłosili zmniejszenie zdolności w czasie u 32% osób z RSTS i pogorszenie zachowania u 37% pacjentów z RSTS, co jest zgodne z raportem Hennekam i wsp. z 1992 roku. W związku z tym ważna jest dalsza opieka w celu identyfikacji i leczenia problemów psychiatrycznych, które pojawiają się wraz z wiekiem. Wreszcie, częstość występowania RSTS może być wyższa niż pierwotnie szacowana z powodu późnej diagnozy, szczególnie w łagodniejszych przypadkach.
Podejścia diagnostyczne
Osoby z podejrzeniem RSTS powinny być oceniane przez genetyków dziecięcych znających się na dysmorfologii. Szereg technik molekularnych jest szeroko stosowanych w analizach genetycznych RSTS. Wśród tych badań, analiza kariotypu może wykazać rzadkie, widoczne cytogenetycznie nieprawidłowości (translokacje, inwersje lub delecje); chociaż wynik jest zazwyczaj prawidłowy, ocena ta powinna być w każdym przypadku przeprowadzona w celu identyfikacji możliwych rearanżacji. FISH może zidentyfikować mikrodelecje, przy czym wskaźnik wykrywalności wynosi 5-10%. Badanie analizy delecji/duplikacji identyfikuje delecje/duplikacje egzoniczne lub w całym genie, które nie są wykrywalne przez analizę sekwencji kodujących i flankujących intronowych regionów genomowego DNA. Można zastosować różne metody (ilościowa PCR, PCR dalekiego zasięgu, multiplex ligation-dependent probe amplification (MLPA), mikromacierz chromosomalna). Stef i wsp. wykryli delecje u 17 (20,5%) z 83 pacjentów przy użyciu array-CGH i ilościowego multipleksowego fluorescencyjnego PCR. Analiza molekularna pozwala również na identyfikację mutacji w genach CREBBP i EP300. Patogenne warianty genu CREBBP zostały zidentyfikowane u 50-70% osób z RSTS, podczas gdy mutacje w genie EP300 zostały opisane u około 5-8% pacjentów z RSTS przez Roelfsema et al. , Bartholdi et al. , Negri et al.
Korelacje genotyp-fenotyp
Niewiele wiadomo na temat korelacji genotyp-fenotyp RSTS. Stwierdzono ciężki fenotyp u pacjentów z RSTS z dużymi delecjami, ale inne badania nie potwierdzają tego związku genotypowo-fenotypowego. Jednakże, możliwe jest powiązanie niższego IQ i cech autystycznych z dużymi delecjami u pacjentów z RSTS. Dlatego Calì i wsp. zalecają MLPA, która może zidentyfikować te duże delecje do badań przesiewowych pacjentów z RSTS z niższym IQ i cechami autystycznymi. Mutacje poza domeną acetylotransferazy histonowej (HAT) były związane z łagodnym fenotypem. Ponadto, mozaicyzm somatyczny może być również związany z łagodnym RSTS . Do tej pory zidentyfikowano i scharakteryzowano mniej niż 20 pacjentów z RSTS z mutacjami EP300. Mutacje EP300 są związane ze stanem przedrzucawkowym u kobiet noszących ciążę dotkniętą RSTS; opisano zajęcie skóry i łagodny fenotyp w nieprawidłowościach szkieletowych i problemach neuropsychiatrycznych.
Poradnictwo genetyczne
Większość przypadków RSTS jest sporadyczna i tylko kilka przypadków RSTS dotyczących rodzeństwa zostało zgłoszonych do tej pory. Transmisja wertykalna jest niezwykle rzadka. Chociaż ryzyko nawrotu RSTS jest generalnie niskie, należy zapewnić odpowiednie doradztwo genetyczne w celu prenatalnej diagnostyki RSTS. Na przykład, mozaikowatość somatyczna została potwierdzona u klinicznie niedotkniętego chorobą ojca chłopca z RSTS oraz u łagodnie dotkniętego chorobą ojca trzech kobiet z RSTS. Ponadto, mozaicyzm germinalny był hipotezą w dwóch przypadkach RSTS . W oparciu o te doniesienia, ryzyko nawrotu RSTS wynosi około 0,5-1%.
Zarządzanie
Pomimo znacznego postępu w wiedzy na temat objawów klinicznych i historii naturalnej RSTS, wytyczne dotyczące opieki zdrowotnej i kontynuacji leczenia RSTS nie zostały dobrze zaktualizowane po propozycji Wiley i wsp. w 2003 roku (Tabela 2). Nowe terapie genetyczne i epigenetyczne mogą być obiecującymi metodami leczenia RSTS, ale istnieje pilna potrzeba poprawy i personalizacji standardowego protokołu obserwacji. Na podstawie naszej wiedzy i krytycznych aspektów, które omawiamy poniżej, opracowaliśmy naszą propozycję postępowania uzupełniającego (Tabela 3).
Postępowanie powinno być dostosowane w wieku młodzieńczym, ze względu na znane różnice w niektórych kwestiach (cechy okulistyczne, skłonność do otyłości i zaburzenia nastroju w szczególności).
Nieznane i krytyczne zagadnienia w RSTS
Osiągnięto znaczny postęp w badaniach nad podłożem genetycznym i zagadnieniami medycznymi RSTS, co przyczynia się do wstępnej diagnozy klinicznej i późniejszego potwierdzenia poprzez analizy molekularne. Biorąc pod uwagę złożoność i rzadkość tego zespołu, nadal istnieje wiele pytań dotyczących RSTS, na które nie ma odpowiedzi. Dlatego też dalsze badania powinny koncentrować się na diagnostyce klinicznej i postępowaniu, jak również na korelacji genotyp-fenotyp.
W oparciu o nasze doświadczenie, nieprawidłowe wzorce wzrostu widoczne na standardowych wykresach wzrostu powinny być podkreślone w kryteriach diagnostycznych RSTS. Ponadto, kliniczne kryteria diagnostyczne i badania przesiewowe mogą być dalej klasyfikowane w zależności od okresu prenatalnego, dziecięcego i młodzieńczego. W szczególności obecność prawidłowego wzrostu in utero, w połączeniu z innymi markerami, takimi jak szerokie kciuki/halluzy i inne wady rozwojowe, jest przydatna w diagnostyce różnicowej RSTS z innymi zespołami (np. zespołem Cornelii de Lange). Genetycy dziecięcy powinni zwrócić większą uwagę na poszerzone paliczki dystalne: przeglądając zdjęcia pacjentów przesłane do analiz molekularnych, w zdecydowanej większości przypadków stwierdziliśmy ten objaw, nie odnotowany w kartach klinicznych. Powiększony pierwszy palec jest cechą powszechnie znaną, ale także powszechną w innych zespołach, takich jak akrocefalopolisndaktylia, podczas gdy konformacja paliczków dystalnych wydaje się być bardziej specyficzna dla RSTS. Co więcej, często pomijane talony są również wysoce specyficzne dla RSTS. Ze względu na liczne doniesienia oraz znaczenie diagnostyczne i prognostyczne tych cech konieczne jest przeprowadzenie wieloośrodkowego badania częstości występowania nieprawidłowości w obrębie mózgu i kręgosłupa; przesiewowe badanie MRI mózgu/czaszki mogłoby być przydatne jako uzupełnienie podstawowej diagnostyki. Ponadto, jeśli chodzi o cechy endokrynologiczne, ostatnio dodano więcej informacji dotyczących w szczególności kształtu i funkcji tarczycy, a osobiście znamy dwa inne przypadki z łagodną niedoczynnością tarczycy i małą tarczycą. Oprócz niepełnosprawności intelektualnej, u pacjentów z RSTS znane są pewne zmiany behawioralne, ale brak jest istotnych dowodów potwierdzających wartość diagnostyczną tych cech neuropsychiatrycznych w diagnostyce RSTS. Dlatego też, żadne cechy neuropsychiatryczne nie są wystarczająco silne, aby włączyć je do kryteriów diagnostycznych RSTS, chociaż niektóre cechy mogą bardziej sugerować mutacje EP300. W tych przypadkach ID jest łagodne lub nieobecne, a dominują zaburzenia zachowania (np. lęk). Inne cechy sugerujące mutacje EP300 obejmują stan przedrzucawkowy i mniej znaczące nieprawidłowości w pierwszej cyfrze, co stanowi wskazówkę do sporządzenia kryteriów różnicujących dla EP300 oraz do bardziej precyzyjnego i zindywidualizowanego schematu laboratoryjnego. Według naszej najlepszej wiedzy jest to jedyna możliwa zmiana w kolejności badań molekularnych, ponieważ inne korelacje genotyp-fenotyp są jedynie orientacyjne. W trakcie dalszej opieki nad RSTS mogą wystąpić liczne niespecyficzne powikłania, dlatego trudno jest ustalić ogólny i skuteczny protokół dalszego postępowania. Ponadto, nie zidentyfikowano silnych korelacji genotyp-fenotyp. Ogólnie rzecz biorąc, należy skupić się na obserwacji ortopedycznej, monitorowaniu diety w okresie dojrzewania i w okresie neuropsychiatrycznym oraz ocenie okulistycznej u dorosłych. Mniej rygorystyczny protokół obserwacji może być odpowiedni tylko dla pacjentów z RSTS z mutacją EP300, ze szczególnym uwzględnieniem problemów skórnych (pilomatrixoma i znamiona), które prawdopodobnie występują częściej niż u pacjentów z mutacją CREBBP. Jeśli chodzi o poradnictwo genetyczne, badanie śliny i testy genetyczne są ważne dla oceny ryzyka nawrotu u rodziców z mozaikowatością germinalną i somatyczną.
Dyskusja na temat krytycznych aspektów postępu w zrozumieniu etiopatogenezy RSTS jest poza zakresem tego przeglądu, ale różne modele mysie zostały stworzone z interesującymi wynikami.

