Daratumumab (DARA) es un medicamento recientemente aprobado por la FDA y patentado por Janssen para el tratamiento del mieloma múltiple. Este fármaco es un anticuerpo monoclonal (MoAb) lgG1k dirigido a CD38 que se expresa en las células del mieloma; es altamente citotóxico para las células tumorales de estos pacientes.1-4 La presencia del antígeno CD38 en las superficies de los eritrocitos de individuos sanos también se ha demostrado por citometría de flujo.5 Además, se ha detectado panreactividad en el plasma de pacientes tratados con DARA en pruebas de compatibilidad rutinarias.6 Este es un nuevo problema en la medicina transfusional que retrasa la entrega oportuna de componentes sanguíneos, lo que representa un peligro potencial para la vida del paciente. Siendo un tema de reciente aparición, los manuales de procedimientos técnicos (es decir, la AABB), no contemplan una metodología específica para la resolución de este tipo de problemas.
Desde hace más de 20 años, el tratamiento de los hematíes con el agente redox ditiotreitol (DDT) se ha utilizado comúnmente para desnaturalizar el antígeno Kell, así como otros grupos de antígenos menos significativos desde el punto de vista clínico como resultado de una reacción hemolítica transfusional. Podemos ver esto como en los casos de Landsteiner-Wiener, Cartwright, Dombrock, Indian, Jhon Milton Hagen, Lutheran y Raph. Esta característica es útil en la investigación de aloanticuerpos (manual técnico de la AABB).7,8
Más recientemente, se ha demostrado que el antígeno CD38 también es sensible a la desnaturalización mediante el agente redox ditiotreitol (DDT),9 sin afectar al resto de los antígenos eritrocitarios clínicamente significativos. Entre las posibilidades para erradicar la interferencia, aplicamos la técnica del DTT, que permite detectar la presencia de anticuerpos clínicamente significativos, proporcionando así componentes sanguíneos con un menor riesgo transfusional para el paciente.
Materiales y métodos
El banco de sangre del hospital Zambrano Hellion recibió una solicitud de transfusión de 2 unidades de paquetes globulares y 4 concentrados de plaquetas. El paciente, un varón de 64 años sin transfusiones en su historial, tenía un diagnóstico de mieloma múltiple de 4 años de evolución y era resistente al tratamiento médico convencional. Se extrajo sangre venosa con EDTA. Las muestras se estudiaron para las pruebas rutinarias de pretransfusión mediante los métodos y técnicas convencionales utilizados en el banco de sangre (es decir, técnicas de microaglutinación en gel). Los estudios de grupo sanguíneo ABO y Rh se realizaron con tarjetas Grifols.
Para el seguimiento e identificación de anticuerpos irregulares, se utilizó un panel completo de eritrocitos Grifols, así como columnas de Coombs en gel Grifols DG. Además, las pruebas de compatibilidad cruzada previas a la transfusión se procesaron de acuerdo con la técnica descrita en el inserto de DG Coombs (antiglobulina poliespecífica), para el tratamiento de los eritrocitos con ditiotreitol (DTT) a 0,2M, pH 8, utilizando el método 4.6 del manual técnico del ABB (12ª edición de las secciones de métodos generales de laboratorio)8 (véase la Fig. 1).
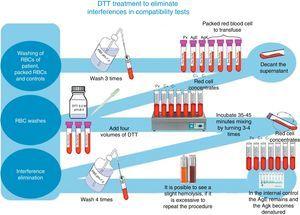
Tratamiento con TDT para eliminar las interferencias en las pruebas de compatibilidad.
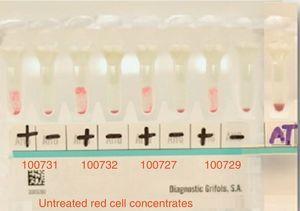
Main cross matching test with 4 donors resulted in incompatibility. Positive=main crossmatching (+), negative=minor crossmatching (−), AT=auto-control crossmatch.
The main cross-matching test resulted in incompatibility with all studied donors (15 in total).
The patient’s erythrocytes presented a negative direct anti-human globulin test (IgG and C3b), as well as a negative control. The presence of hemolysis in the patient’s sample was not detected (see Fig. 3).

Results direct anti-human globulin test (IgG and C3b) presenting negative results.
En el momento de realizar las pruebas con el plasma del paciente y los eritrocitos previamente tratados con DTT de los diferentes donantes, así como los utilizados en el panel de cribado de anticuerpos, no encontramos reactividad en ninguna de las muestras estudiadas. Se utilizaron eritrocitos de control K+ y E+ para verificar que el DTT desnaturalizaba únicamente el antígeno K y preservaba el antígeno E; esto formaba parte del control de calidad de nuestro estudio para determinar que otros antígenos relacionados con anticuerpos clínicamente significativos estaban inactivos (véase la Fig. 4).

Panel de cribado de anticuerpos eritrocitarios DTT triado, mostrando resultados negativos en 4 donantes de sangre. C1 (control positivo) C2 (control negativo).
Discusión
Hay pruebas de que los anti-CD38 en el suero de los pacientes tratados con DARA se unen con el antígeno CD38 expresado en los eritrocitos utilizados en el panel de rastreo de anticuerpos, así como en los donantes de la prueba de compatibilidad cruzada previa a la transfusión, generando una panreactividad. Esto puede enmascarar la presencia de anticuerpos clínicamente significativos, especialmente en pacientes multíparas o en pacientes politransfundidos. Esta pan-reactividad puede revertirse mediante el uso de agentes neutralizantes, que restablecen la identificación de anticuerpos irregulares y las pruebas de rastreo. Los anticuerpos antiidiotipo, así como el CD38 recombinante soluble, han sido evaluados en artículos anteriores con resultados positivos.
De las posibilidades disponibles para eliminar esta interferencia en el banco de sangre, utilizamos la técnica del DDT. Su mejor característica es el hecho de que se trata de un agente redox que interrumpe la estructura terciaria de la proteína mediante la reducción irreversible de los enlaces disulfuro a sulfhidrilo libre. Sin una estructura terciaria, los antígenos, que contienen proteínas, ya no pueden fijar anticuerpos, inhibiendo así la reactividad serológica. Un problema potencial de esta técnica es que también afecta a otros antígenos del grupo sanguíneo. Sin embargo, en la práctica diaria, sólo el antígeno K es clínicamente significativo. Por lo tanto, se recomienda que los pacientes tratados con DARA sólo sean transfundidos con concentrados de eritrocitos K. También existe la posibilidad de perder la reactividad a otros agentes como el K y el Yta. Sin embargo, esto resulta ser un evento extremadamente raro. El DDT no desactiva la actividad serológica de la mayoría de los antígenos clínicamente significativos y frecuentes como los sistemas Rh, Duffy, Kidd y MNS. Es prudente determinar el fenotipo o genotipo del paciente antes de iniciar el tratamiento con DARA.
En Inmunohematología preocupa el posible aumento de este tipo de interferencias en las pruebas rutinarias de transfusión sanguínea, que pueden surgir como consecuencia de las nuevas terapias con anticuerpos monoclonales en pacientes con cáncer.
En conclusión, nuestro estudio demostró que el tratamiento de los eritrocitos con TDT inactiva el antígeno CD38, eliminando la reactividad con el suero del paciente tratado con DARA. Este método sencillo y práctico permite realizar estudios sin las interferencias que la presencia de aloanticuerpos puede provocar en las reacciones transfusionales de los pacientes que reciben una terapia basada en este anticuerpo monoclonal.
El problema de la panreactividad que provoca interferencias en las pruebas de compatibilidad de los pacientes tratados con DARA puede resolverse técnicamente con el tratamiento de los eritrocitos con DTT de los potenciales donantes de sangre. Este agente desactiva el antígeno CD38 presente en estas células. Esta panreactividad no debe retrasar la entrega de los productos sanguíneos, que en situaciones de emergencia serán utilizando paquetes globulares ABO idénticos y hematíes Rh compatibles, según las prácticas del banco de sangre. Esto, obliga a generar recomendaciones y/o guías a los médicos tratantes y al personal de los bancos de sangre que atienden a este tipo de pacientes. Es importante considerar que, hasta la fecha, no se han observado reacciones hemolíticas transfusionales en los aproximadamente 2000 pacientes que han sido tratados con DARA.8 Investigaciones recientes sobre la seguridad transfusional en pacientes tratados con DARA que comprenden alrededor de 76.000 ciclos de aplicación del fármaco no encontraron ni una sola reacción adversa a la hemólisis transfusional.10-12
El trabajo conjunto del onco-hematólogo y el banco de sangre debe estar presente desde el momento en que los pacientes ingresan al hospital. Los procedimientos de transfusión aplicados a este tipo de pacientes deben incluir la identificación del fenotipo eritrocitario completo de la caja con su grupo sanguíneo, y las pruebas de compatibilidad deben realizarse en la medida de nuestras posibilidades antes de la aplicación de este medicamento.
La técnica de desactivación de TDT descrita anteriormente representa una medida alternativa de seguridad transfusional en todos los casos. Nuestro banco de sangre es pionero en nuestro país en la adopción de esta tecnología recientemente descrita y validada internacionalmente.13 Sin embargo, en situaciones críticas de emergencia transfusional donde la vida del paciente está en peligro, sólo se debe transfundir sangre con compatibilidad ABO y RhD, sin realizar las pruebas de compatibilidad según las políticas y procedimientos previamente descritos en las transfusiones de emergencia.
Conflicto de intereses
Los autores no tienen ningún conflicto de intereses que declarar.