Takeaways
-
A Google tulajdonában lévő DeepMind laboratórium “deep learning” szoftverprogramja nagy előrelépést mutatott a biológia egyik legnagyobb kihívásának – a fehérjék hajtogatásának megértésében.
-
A fehérjék hajtogatása az a folyamat, amelynek során egy fehérje az építőelemek sorából felveszi alakját a végső háromdimenziós szerkezetéig, amely meghatározza a funkcióját.
-
Azáltal, hogy jobban megjósolható, hogyan veszik fel a fehérjék a szerkezetüket, vagyis “hajtogatják”, a tudósok gyorsabban tudnak olyan gyógyszereket kifejleszteni, amelyek például blokkolják a kulcsfontosságú vírusfehérjék működését.
A biológusok által “a fehérje-összecsukódási problémának” nevezett feladat megoldása nagy dolog. A fehérjék a sejtek munkagépei, és minden élő szervezetben jelen vannak. Aminosavak hosszú láncaiból állnak, és létfontosságúak a sejtek felépítéséhez és a sejtek közötti kommunikációhoz, valamint a szervezet összes kémiai folyamatának szabályozásához.
A héten a Google tulajdonában lévő DeepMind mesterséges intelligenciával foglalkozó vállalat bemutatta az AlphaFold2 nevű mélytanuló programot, amelyet a szakértők áttörésnek neveznek a fehérjék hajtogatásának nagy kihívásának megoldása felé.
A fehérjék aminosavak hosszú láncai, amelyek úgy kapcsolódnak egymáshoz, mint gyöngyök a madzagon. Ahhoz azonban, hogy egy fehérje elvégezze a feladatát a sejtben, “össze kell hajtogatnia” – ez egy olyan csavarodási és hajlítási folyamat, amely a molekulát egy összetett háromdimenziós szerkezetté alakítja át, amely képes kölcsönhatásba lépni a sejtben lévő célpontjával. Ha a hajtogatás megszakad, akkor a fehérje nem fogja a megfelelő alakot kialakítani – és nem lesz képes ellátni a feladatát a szervezetben. Ez betegséghez vezethet – ahogyan az olyan gyakori betegségeknél, mint az Alzheimer-kór, és olyan ritka betegségeknél, mint a cisztás fibrózis.
A mélytanulás olyan számítási technika, amely a hatalmas adathalmazokban rejlő, gyakran rejtett információkat használja fel az érdekes kérdések megoldására. Széles körben alkalmazzák olyan területeken, mint a játékok, a beszéd- és hangfelismerés, az autonóm autók, a tudomány és az orvostudomány.
Hiszem, hogy az olyan eszközök, mint az AlphaFold2, segíteni fogják a tudósokat új típusú fehérjék tervezésében, olyanokéban, amelyek például segíthetnek a műanyagok lebontásában és a jövőbeli vírusjárványok és betegségek elleni küzdelemben.
Számítógépes kémikus vagyok, és a The State of Science című könyv szerzője. Tanítványaimmal a fluoreszcens fehérjék szerkezetét és tulajdonságait tanulmányozzuk a klasszikus fizikán alapuló fehérje-hajtogató számítógépes programok segítségével.
A több ezer kutatócsoport több évtizedes tanulmányozása után ezek a fehérje-összecsukódást előrejelző programok nagyon jól kiszámítják azokat a szerkezeti változásokat, amelyek akkor következnek be, ha ismert molekulákon kis változtatásokat hajtunk végre.
De még nem sikerült megfelelően megjósolniuk, hogyan hajtódnak össze a fehérjék a semmiből. A mélytanulás megjelenése előtt a fehérje-hajtogatás problémája lehetetlenül nehéznek tűnt, és úgy tűnt, hogy még évtizedekig frusztrálni fogja a számítógépes kémikusokat.
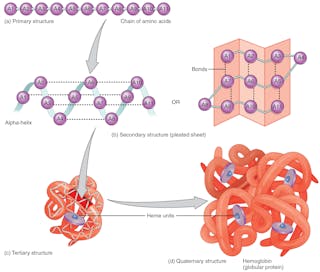
A fehérje hajtogatása
A fehérje 3D alakját az aminosavak – DNS-ben kódolt – sorrendje határozza meg. Az alak határozza meg a funkcióját. Ha a fehérje szerkezete megváltozik, nem tudja ellátni a funkcióját. A fehérjék hajtogatásának az aminosav-szekvencia alapján történő helyes előrejelzése forradalmasíthatja a gyógyszertervezést, és magyarázatot adhat az új és régi betegségek okaira.
Az aminosav-építőelemek azonos szekvenciájával rendelkező fehérjék mindegyike ugyanabba a háromdimenziós formába hajtódik, ami optimalizálja az aminosavak közötti kölcsönhatásokat. Ezt ezredmásodpercek alatt teszik meg, noha csillagászati számú lehetséges konfiguráció áll rendelkezésükre – körülbelül 10 a 300 hatványán. Ez a hatalmas szám az, ami miatt nehéz megjósolni, hogyan hajtódik össze egy fehérje, még akkor is, ha a tudósok ismerik a fehérje előállításához szükséges aminosavak teljes szekvenciáját. Korábban lehetetlen volt megjósolni a fehérje szerkezetét az aminosavak szekvenciájából. A fehérjék szerkezetét kísérleti úton határozták meg, ami időigényes és költséges vállalkozás volt.
Ha a kutatók jobban meg tudják jósolni, hogyan hajtogatódnak össze a fehérjék, jobban meg tudják majd érteni, hogyan működnek a sejtek, és hogyan okoznak betegségeket a rosszul hajtogatott fehérjék. A jobb fehérje-előrejelző eszközök segítenek majd olyan gyógyszerek tervezésében is, amelyek a fehérje egy adott topológiai régióját célozzák meg, ahol a kémiai reakciók lezajlanak.

Az AlphaFold a mélytanuló sakk-, Go és pókerjátékokból született
A DeepMind AlphaFold nevű, fehérjék hajtogatását előrejelző programjának sikere nem váratlan. A DeepMind által írt más mélytanuló programok a világ legjobb sakk-, Go és pókerjátékosait verték le.
2016-ban a Stockfish-8, egy nyílt forráskódú sakkmotor lett a számítógépes sakkvilágbajnok. Másodpercenként 70 millió sakkpozíciót értékelt ki, és évszázadok felhalmozott emberi sakkstratégiáira, valamint évtizedes számítógépes tapasztalatra támaszkodhatott. Hatékonyan és brutálisan játszott, kíméletlenül legyőzve minden emberi kihívóját egy cseppnyi finomság nélkül. Jöjjön a mélytanulás.
2017. december 7-én a Google AlphaZero nevű mélytanuló sakkprogramja legyőzte a Stockfish-8-at. A sakkmotorok 100 partit játszottak, amelyek közül az AlphaZero 28-at megnyert, 72-ben pedig döntetlent ért el. Egyetlen játszmát sem veszített. Az AlphaZero másodpercenként mindössze 80 000 számítást végzett, szemben a Stockfish-8 70 millió számításával, és mindössze négy óra alatt tanult meg sakkozni a semmiből úgy, hogy néhány milliószor játszott saját maga ellen, és a tapasztalatokból tanulva optimalizálta neurális hálózatait.
Az AlphaZero semmit sem tanult az emberektől vagy az emberek által játszott sakkjátszmáktól. Saját magát tanította, és eközben soha nem látott stratégiákat fejlesztett ki. A Science magazinban megjelent kommentárjában Garri Kaszparov korábbi sakkvilágbajnok azt írta, hogy az AlphaZero a saját játékából tanulva olyan stratégiákat fejlesztett ki, amelyek “a sakk igazságát” tükrözik, nem pedig a programozók “prioritásait és előítéleteit”. “Ez a ‘dolgozz okosabban, ne keményebben’ közhely megtestesítője.”
CASP – a molekulamodellezők olimpiája
Kétévente a világ legjobb számítógépes kémikusai tesztelik a fehérjék hajtogatását előrejelző programjaik képességeit, és versenyeznek a Critical Assessment of Structure Prediction (CASP) versenyen.
A versenyen a csapatok mintegy 100 olyan fehérje aminosavainak lineáris szekvenciáját kapják meg, amelyek 3D alakja ismert, de még nem publikálták; ezután ki kell számítaniuk, hogyan hajtódnának össze ezek a szekvenciák. 2018-ban az AlphaFold, a verseny mélytanulási újonca az összes hagyományos programot legyőzte – de alig-alig.
Két évvel később, hétfőn jelentették be, hogy az Alphafold2 szép fölénnyel megnyerte a 2020-as versenyt. Legyőzte versenytársait, és előrejelzései összehasonlíthatóak voltak a meglévő kísérleti eredményekkel, amelyeket olyan arany standard technikákkal határoztak meg, mint a röntgendiffrakciós kristallográfia és a krio-elektronmikroszkópia. Arra számítok, hogy hamarosan az AlphaFold2 és utódai lesznek a fehérjék szerkezetének meghatározására használt módszerek, mielőtt olyan kísérleti technikákhoz folyamodnánk, amelyek fáradságos, fáradságos munkát igényelnek drága műszerekkel.
Az AlphaFold2 sikerének egyik oka az, hogy a több mint 170 000 kísérletileg meghatározott 3D szerkezetet tartalmazó Protein Database-t használhatta arra, hogy betanítsa magát a fehérjék helyesen hajtogatott szerkezetének kiszámítására.
Az AlphaFold potenciális hatását akkor lehet értékelni, ha összehasonlítjuk az összes közzétett fehérjeszerkezet számát – körülbelül 170 000 – az egyetemes fehérjeadatbázisban letétbe helyezett 180 millió DNS- és fehérjeszekvenciával. Az AlphaFold segít majd átválogatni a DNS-szekvenciák kincsesbányáját, új, egyedi szerkezetű és funkciójú fehérjékre vadászva.
Ha az AlphaFold feleslegessé tett engem, a molekulamodellezőt?
Mint a sakk és a Go programok – AlphaZero és AlphaGo – esetében, nem tudjuk pontosan, mit csinál az AlphaFold2 algoritmus, és miért használ bizonyos összefüggéseket, de azt tudjuk, hogy működik.
Amellett, hogy segít megjósolni a fontos fehérjék szerkezetét, az AlphaFold “gondolkodásának” megértése segít abban is, hogy új betekintést nyerjünk a fehérjék hajtogatásának mechanizmusába.
Az egyik leggyakrabban hangoztatott félelem az AI-val kapcsolatban, hogy az nagymértékű munkanélküliséghez fog vezetni. Az AlphaFoldnak még jelentős utat kell megtennie ahhoz, hogy következetesen és sikeresen meg tudja jósolni a fehérjék hajtogatását.
Mihelyt azonban kiforrott, és a program képes lesz a fehérjék összecsukódását szimulálni, a számításos kémikusok szerves részesei lesznek a programok tökéletesítésének, megpróbálják megérteni az alkalmazott összefüggéseket, és alkalmazzák a programot olyan fontos problémák megoldására, mint a számos betegséggel, például az Alzheimer-kórral, a Parkinson-kórral, a cisztás fibrózissal és a Huntington-kórral összefüggő fehérje-hibás összecsukódás.
Az AlphaFold és utódai minden bizonnyal megváltoztatják majd a számítógépes kémikusok munkáját, de nem teszik őket feleslegessé. Más területek nem lesznek ilyen szerencsések. A múltban a robotok képesek voltak helyettesíteni a fizikai munkát végző embereket; a mesterséges intelligenciával a kognitív képességeink is kihívást jelentenek.