Zážitky
-
Softwarový program „deep learning“ z laboratoře DeepMind, která patří společnosti Google, prokázal velký pokrok při řešení jedné z největších výzev biologie – pochopení skládání proteinů.
-
Skládání bílkovin je proces, při kterém bílkovina získává svůj tvar z řetězce stavebních bloků až do konečné trojrozměrné struktury, která určuje její funkci.
-
Díky lepší předpovědi toho, jak bílkoviny získávají svou strukturu neboli „skládání“, mohou vědci rychleji vyvíjet léky, které například blokují působení klíčových virových bílkovin.
Vyřešení toho, čemu biologové říkají „problém skládání proteinů“, je velká věc. Proteiny jsou pracovními koňmi buněk a jsou přítomny ve všech živých organismech. Jsou tvořeny dlouhými řetězci aminokyselin a mají zásadní význam pro strukturu buněk a komunikaci mezi nimi a také pro regulaci veškeré chemie v těle.
Tento týden předvedla společnost DeepMind, vlastněná společností Google, program pro hluboké učení nazvaný AlphaFold2, který odborníci označují za průlom směrem k vyřešení velkého problému skládání proteinů.
Bílkoviny jsou dlouhé řetězce aminokyselin spojených dohromady jako korálky na šňůrce. Aby však bílkovina mohla v buňce plnit svou úlohu, musí se „složit“ – jedná se o proces kroucení a ohýbání, který přemění molekulu na složitou trojrozměrnou strukturu, která může interagovat se svým cílem v buňce. Pokud je skládání narušeno, pak protein nevytvoří správný tvar – a nebude schopen plnit svou práci v těle. To může vést k onemocnění – jako je tomu v případě běžného onemocnění, jako je Alzheimerova choroba, a vzácných onemocnění, jako je cystická fibróza.
Hluboké učení je výpočetní technika, která využívá často skryté informace obsažené v rozsáhlých souborech dat k řešení zajímavých otázek. Hojně se využívá v oborech, jako jsou hry, rozpoznávání řeči a hlasu, autonomní automobily, věda a medicína.
Věřím, že nástroje jako AlphaFold2 pomohou vědcům navrhnout nové typy proteinů, které mohou například pomoci rozkládat plasty a bojovat proti budoucím virovým pandemiím a nemocem.
Jsem počítačový chemik a autor knihy Stav vědy. Se svými studenty studuji strukturu a vlastnosti fluorescenčních proteinů pomocí počítačových programů pro skládání proteinů založených na klasické fyzice.
Po desetiletích studia tisíců výzkumných skupin jsou tyto programy pro předpověď skládání proteinů velmi dobré ve výpočtu strukturních změn, ke kterým dochází, když provedeme malé změny známých molekul.
Nedokázaly však dostatečně předpovědět, jak se proteiny skládají od nuly. Než se objevilo hluboké učení, zdál se problém skládání proteinů nemožně obtížný a zdálo se, že bude frustrovat výpočetní chemiky po mnoho dalších desetiletí.
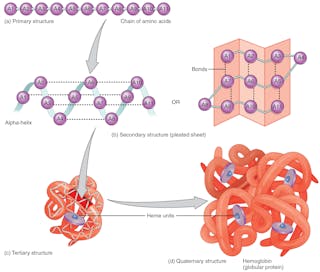
Skládání bílkovin
Pořadí aminokyselin – které je zakódováno v DNA – určuje 3D tvar bílkoviny. Tvar určuje jeho funkci. Pokud se struktura proteinu změní, není schopen plnit svou funkci. Správná předpověď skládání proteinů na základě sekvence aminokyselin by mohla přinést revoluci v navrhování léků a vysvětlit příčiny nových i starých nemocí.
Všechny bílkoviny se stejnou sekvencí stavebních bloků aminokyselin se skládají do stejné trojrozměrné formy, která optimalizuje interakce mezi aminokyselinami. Dělají to během milisekund, přestože mají k dispozici astronomický počet možných konfigurací – přibližně 10 na mocninu 300. V tomto případě se jedná o tzv. Díky tomuto obrovskému počtu je obtížné předpovědět, jak se protein složí, i když vědci znají celou sekvenci aminokyselin, které se na jeho tvorbě podílejí. Dříve bylo předvídání struktury bílkovin ze sekvence aminokyselin nemožné. Struktura bílkovin se určovala experimentálně, což bylo časově náročné a nákladné.
Jakmile budou vědci schopni lépe předpovědět, jak se proteiny skládají, budou moci lépe pochopit, jak buňky fungují a jak chybně složené proteiny způsobují nemoci. Lepší nástroje pro předpovídání proteinů nám také pomohou navrhnout léky, které se mohou zaměřit na konkrétní topologickou oblast proteinu, kde probíhají chemické reakce.

AlphaFold se zrodil z hlubokého učení šachů, hry Go a pokeru
Úspěch programu společnosti DeepMind pro předpovídání skládání proteinů s názvem AlphaFold není nečekaný. Jiné programy pro hluboké učení napsané společností DeepMind zničily nejlepší světové hráče šachu, Go a pokeru
V roce 2016 se stal světovým počítačovým šachovým šampionem Stockfish-8, šachový engine s otevřeným zdrojovým kódem. Vyhodnotil 70 milionů šachových pozic za sekundu a měl k dispozici staletí nashromážděných lidských šachových strategií a desítky let počítačových zkušeností, ze kterých mohl čerpat. Hrál efektivně a brutálně a nemilosrdně porážel všechny své lidské vyzyvatele bez špetky jemnosti. Nastupuje hluboké učení.
Dne 7. prosince 2017 šachový program AlphaZero společnosti Google využívající hluboké učení porazil šachistu Stockfish-8. Šachové motory sehrály 100 partií, přičemž AlphaZero vyhrál 28 a 72 remizoval. Neprohrál ani jednu partii. AlphaZero provedl pouze 80 000 výpočtů za sekundu oproti 70 milionům výpočtů programu Stockfish-8. Naučit se šachy od začátku mu trvalo pouhé čtyři hodiny, když hrál sám proti sobě několik milionkrát a optimalizoval své neuronové sítě, jak se učil ze svých zkušeností.
AlphaZero se nic nenaučil od lidí ani z šachových partií hraných lidmi. Učilo se samo a přitom odvodilo dosud nevídané strategie. Bývalý mistr světa v šachu Garry Kasparov v komentáři v časopise Science napsal, že díky tomu, že se AlphaZero učil ze své vlastní hry, vyvinul strategie, které „odrážejí pravdu“ o šachu, a nikoli „priority a předsudky“ programátorů. „Je to ztělesnění klišé ‚pracuj chytřeji, ne tvrději‘.“
CASP – olympiáda pro molekulární modeláře
Každé dva roky nejlepší světoví počítačoví chemici testují schopnosti svých programů předpovídat skládání proteinů a soutěží v soutěži Critical Assessment of Structure Prediction (CASP).
V soutěži dostanou týmy lineární sekvence aminokyselin pro přibližně 100 proteinů, jejichž 3D tvar je znám, ale dosud nebyl publikován; poté musí vypočítat, jak by se tyto sekvence složily. V roce 2018 AlphaFold, nováček v soutěži s hlubokým učením, porazil všechny tradiční programy – ale jen těsně.
O dva roky později, v pondělí, bylo oznámeno, že Alphafold2 zvítězil v soutěži pro rok 2020 se zdravým náskokem. Své konkurenty porazil a jeho předpovědi byly srovnatelné s dosavadními experimentálními výsledky určenými pomocí zlatých standardních technik, jako je rentgenová difrakční krystalografie a kryoelektronová mikroskopie. Očekávám, že brzy se AlphaFold2 a jeho potomci stanou metodami volby pro určování struktury proteinů předtím, než se uchýlíme k experimentálním technikám, které vyžadují namáhavou a pracnou práci na drahých přístrojích.
Jedním z důvodů úspěchu AlphaFold2 je, že mohl využít databázi proteinů, která obsahuje více než 170 000 experimentálně určených 3D struktur, k tomu, aby se naučil vypočítávat správně složené struktury proteinů.
Potenciální dopad AlphaFold lze ocenit, pokud porovnáme počet všech publikovaných struktur proteinů – přibližně 170 000 – se 180 miliony sekvencí DNA a proteinů uložených v Univerzální databázi proteinů. AlphaFold nám pomůže třídit poklady sekvencí DNA při lovu na nové proteiny s jedinečnou strukturou a funkcí.
Způsobil AlphaFold, že jsem se já, molekulární modelář, stal zbytečným?
Stejně jako u šachových programů a programů Go – AlphaZero a AlphaGo – nevíme přesně, co algoritmus AlphaFold2 dělá a proč používá určité korelace, ale víme, že funguje.
Kromě toho, že nám pomůže předpovídat struktury důležitých proteinů, nám pochopení „myšlení“ AlphaFoldu také pomůže získat nové poznatky o mechanismu skládání proteinů.
Jednou z nejčastěji vyjadřovaných obav z umělé inteligence je, že povede k rozsáhlé nezaměstnanosti. AlphaFold má před sebou ještě značnou cestu, než bude schopen konzistentně a úspěšně předpovídat skládání proteinů.
Jakmile však dozraje a program bude schopen simulovat skládání proteinů, budou se výpočetní chemici integrálně podílet na zdokonalování programů, snažit se porozumět základním používaným korelacím a aplikovat program na řešení důležitých problémů, jako je nesprávné skládání proteinů spojené s mnoha nemocemi, jako je Alzheimerova a Parkinsonova choroba, cystická fibróza a Huntingtonova choroba.
AlphaFold a jeho potomci jistě změní způsob práce výpočetních chemiků, ale neučiní je zbytečnými. Jiné oblasti takové štěstí mít nebudou. V minulosti byli roboti schopni nahradit lidi vykonávající manuální práci, s umělou inteligencí jsou naše kognitivní schopnosti rovněž zpochybňovány.