Daratumumab (DARA) é um medicamento recentemente aprovado pela FDA e patenteado por Janssen para o tratamento do mieloma múltiplo. Este fármaco é um anticorpo monoclonal (MoAb) lgGG1k dirigido para o anticorpo CD38, que é expresso em células do mieloma; é altamente citotóxico para as células tumorais destes doentes.1-4 A presença do antigénio CD38 nas superfícies dos eritrócitos de indivíduos saudáveis também foi comprovada pela citometria de fluxo.5 Além disso, foi detectada panreactividade no plasma de pacientes tratados com DARA em testes de compatibilidade de rotina.6 Este é um novo problema na medicina transfusional que atrasa a entrega atempada de componentes sanguíneos, representando assim um perigo potencial para a vida do paciente. Sendo um tópico de emergência recente, os manuais de procedimentos técnicos (ou seja, o AABB), não contemplam uma metodologia específica para a resolução desses tipos de problemas.
Há mais de 20 anos, o tratamento dos eritrócitos com o ditiotreitol (DDT) do agente redox tem sido comumente utilizado para desnaturar o antígeno de Kell, bem como outros grupos de antígenos menos significativos clinicamente como resultado de uma reação transfusional hemolítica. Podemos ver isto como nos casos de Landsteiner-Wiener, Cartwright, Dombrock, Indian, Jhon Milton Hagen, Lutheran e Raph. Este recurso é útil na pesquisa de aloanticorpos (manual técnico do AABB).7,8
Mais recentemente, o antígeno CD38 também se mostrou sensível à desnaturação pelo agente redox dithiothreitol (DDT),9 sem afetar o restante dos antígenos eritrócitos clinicamente significativos. Entre as possibilidades de erradicar a interferência, aplicamos a técnica TDT, que nos permite detectar a presença de anticorpos clinicamente significativos, fornecendo assim componentes sanguíneos com menor risco transfusional para o doente.
Materiais e métodos
O banco de sangue no hospital Zambrano Hellion recebeu um pedido de transfusão de 2 unidades de embalagens globulares e 4 concentrados de plaquetas. O paciente, um homem de 64 anos de idade sem transfusões na sua origem, tinha um diagnóstico de mieloma múltiplo com uma evolução de 4 anos e era resistente ao tratamento médico convencional. O sangue venoso foi colhido com EDTA. As amostras foram estudadas para testes pré-transfusão de rotina através dos métodos e técnicas convencionais utilizados no banco de sangue (ou seja, técnicas de microaglutinação em gel). Foram realizados estudos de grupo sanguíneo ABO e Rh com cartões Grifols.
Para o rastreamento e identificação de anticorpos irregulares, utilizou-se um painel de eritrócitos Grifols completo, bem como colunas de Grifols DG Gel Coombs. Além disso, testes de cruzamento pré-transfusão foram processados de acordo com a técnica descrita na inserção do DG Coombs (poli específico de globulina anti-humana), para o tratamento de eritrócitos com ditiotreitol (DTT) a 0,2M, pH 8, utilizando o 4.6 método do manual técnico da ABB (12ª edição das seções gerais de métodos laboratoriais)8 (ver Fig. 1).
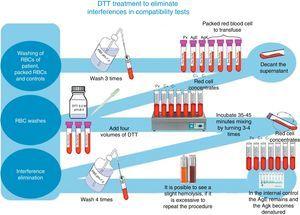
TT tratamento para eliminar interferências nos testes de compatibilidade.
Resultados
p>O plasma do paciente apresentou uma pan-reactividade com os eritrócitos do painel e antígenos conhecidos, que mostraram um padrão de reacção com uma intensidade 3+ (grau 0-4) de forma homogénea (ver Fig. 2).
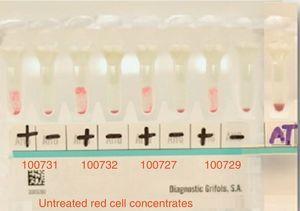
Main cross matching test with 4 donors resulted in incompatibility. Positive=main crossmatching (+), negative=minor crossmatching (−), AT=auto-control crossmatch.
The main cross-matching test resulted in incompatibility with all studied donors (15 in total).
The patient’s erythrocytes presented a negative direct anti-human globulin test (IgG and C3b), as well as a negative control. The presence of hemolysis in the patient’s sample was not detected (see Fig. 3).

Results direct anti-human globulin test (IgG and C3b) presenting negative results.
No momento da realização dos testes com o plasma do paciente e os eritrócitos previamente tratados com TDT dos diferentes doadores, bem como os usados no painel de triagem de anticorpos, não encontramos reatividade em nenhuma das amostras estudadas. Os eritrócitos controle K+ e E+ foram usados para verificar se o TDT desnaturou apenas o antígeno K e preservou o antígeno E; isto fez parte do controle de qualidade do nosso estudo para determinar que outros antígenos relacionados a anticorpos clinicamente significativos estavam inativos (ver Fig. 4).

P>Painel de triagem de anticorpos tratados com TDT, mostrando resultados negativos em 4 doadores de sangue. C1 (controlo positivo) C2 (controlo negativo).
Discussão
O uso do anti-CD38 é um tratamento promissor para doentes com mieloma múltiplo e está actualmente em estudo para outros tipos de neoplasias malignas. O problema é que esta medicação interfere com os testes de compatibilidade, complicando assim a entrega atempada e segura dos componentes sanguíneos.
Existe evidência de que o anti-CD38 no soro dos doentes tratados com DARA liga-se com o antigénio CD38 expresso nos eritrócitos utilizados no painel de rastreio de anticorpos, bem como nos dadores do teste de correspondência cruzada pré-transfusão, gerando uma pan-reactividade. Isto pode mascarar a presença de anticorpos clinicamente significativos, especialmente em pacientes multiparos ou em pacientes poli-transfundidos. Esta pan-reactividade pode ser invertida através do uso de agentes neutralizantes, que restabelecem a identificação irregular dos anticorpos e os testes de rastreio. Anticorpos anti-idiótipo, assim como CD38 recombinante solúvel, foram avaliados em artigos anteriores com resultados positivos.
Das possibilidades disponíveis para eliminar esta interferência no banco de sangue, utilizamos a técnica DDT. Sua melhor característica é o fato de ser um agente redox que interrompe a estrutura terciária da proteína, reduzindo irreversivelmente as ligações de dissulfeto ao sulfidrílico livre. Sem uma estrutura terciária, os antígenos, que contêm proteína, não podem mais fixar anticorpos, inibindo assim a reatividade serológica. Um problema potencial com esta técnica é que ela também afeta os antígenos de outros grupos sanguíneos. No entanto, na prática diária, só o antígeno K é clinicamente significativo. Portanto, é recomendado que os pacientes tratados com DARA só sejam transfundidos com concentrados de K- eritrócitos. A possibilidade de perda de reatividade a outros agentes como K e Yta também está presente. No entanto, este é um evento extremamente raro. O DDT não desactiva a actividade serológica da maioria dos antigénios clinicamente significativos e frequentes, como os sistemas Rh, Duffy, Kidd e MNS. É sensato determinar o fenótipo ou genótipo do paciente antes de iniciar o tratamento com DARA.
Na imuno-hematologia, existe a preocupação com o possível aumento deste tipo de interferência nos testes de transfusão sanguínea de rotina, que pode surgir como consequência de novas terapias com anticorpos monoclonais em pacientes com cancro.
Em conclusão, o nosso estudo demonstrou que o tratamento dos eritrócitos com TDT inactiva o antigénio CD38, eliminando a reactividade com o soro do paciente tratado com DARA. Este método simples e prático permite a realização de estudos sem a interferência que a presença de aloanticorpos pode causar nas reações transfusionais em pacientes que recebem terapia baseada neste anticorpo monoclonal.
O problema da panreatividade que causa interferência nos testes de compatibilidade de pacientes tratados com DARA pode ser tecnicamente resolvido com o tratamento de eritrócitos com TDT de potenciais doadores de sangue. Este agente desativa o antígeno CD38 presente nestas células. Esta panreactividade não deve atrasar a entrega de produtos sanguíneos, que em situações de emergência estarão a utilizar pacotes globulares ABO idênticos e eritrócitos compatíveis com Rh, de acordo com as práticas do banco de sangue. Isto obriga a geração de recomendações e/ou guias para o tratamento de médicos e funcionários dos bancos de sangue que atendem a estes tipos de pacientes. É importante considerar que, até o momento, não foram observadas reações transfusionais hemolíticas nos aproximadamente 2000 pacientes tratados com DARA.8 Pesquisas recentes sobre segurança transfusional em pacientes tratados com DARA, compreendendo cerca de 76.000 ciclos de aplicação de medicamentos, não encontraram uma única reação adversa à hemólise transfusional.10-12
O trabalho conjunto do onco-hematologista e do banco de sangue deve estar presente a partir do momento em que os pacientes são admitidos no hospital. Os procedimentos para transfusão aplicados a estes tipos de pacientes devem incluir a identificação do fenótipo eritrócito completo da caixa com seu grupo sanguíneo, e os testes de compatibilidade devem ser realizados da melhor forma possível antes da aplicação deste medicamento.
A técnica de desativação da TDT descrita acima representa uma medida alternativa de segurança transfusional em todos os casos. Nosso banco de sangue é pioneiro em nosso país na adoção desta tecnologia recentemente descrita e validada internacionalmente.13 No entanto, em situações críticas de emergência transfusional onde a vida do paciente está em perigo, o sangue só deve ser transfundido com compatibilidade ABO e RhD, sem a realização dos testes de compatibilidade de acordo com as políticas e procedimentos previamente descritos em transfusões de emergência.
Conflito de interesse
Os autores não têm conflitos de interesse a declarar.