En elektrolyt är en kemisk förening som dissocieras till joner och därmed kan transportera elektrisk laddning – dvs. en elektrolyt är en elektrisk ledare; till skillnad från metaller är laddningsflödet inte ett flöde av elektroner, utan en rörelse av joner.
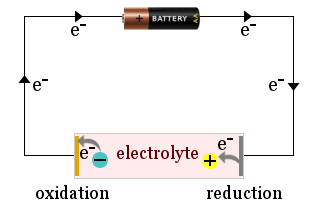
I diagrammet visas till exempel ett hushållsbatteri som används för att locka elektrolytjoner till elektroderna i en elektrokemisk cell, där jonerna får elektroner (reduceras) eller förlorar elektroner (oxideras).
Ibland reagerar själva elektroderna, till exempel kan en metallelektrod oxideras och släppa ut joner i elektrolyten.
Elektrolyter kan vara fasta, vätskor eller lösningar.
Exempel på elektrolyter
1. Smält natriumklorid fungerar som en elektrolyt vid framställning av natriummetall. Klorgas produceras också.
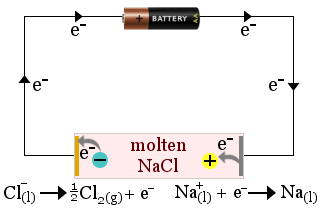 I detta fall förbrukas elektrolyten av cellens redoxreaktioner.
I detta fall förbrukas elektrolyten av cellens redoxreaktioner.
2. Kaliumhydroxid löst i vatten ger en mycket ledande elektrolyt i Edison-cellen, en tidig uppladdningsbar cell.
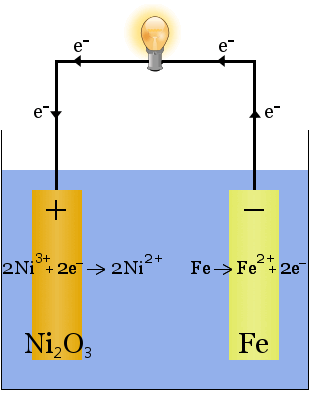
Till skillnad från fallet med natriumproduktion ovan förbrukas ingen elektrolyt i den här reaktionen. kaliumhydroxidens roll i det här fallet är att öka tillgängligheten av joner för att öka elektrolytens ledningsförmåga och sluta den elektriska kretsen.
De kemiska ekvationerna för reaktionerna vid elektroderna är:
För urladdning läses ekvationerna från vänster till höger; för laddning från höger till vänster.
3. Traditionellt sett har elektrolyter varit vätskor för att möjliggöra förflyttning av joner. nu finns det dock fasta material som gör att joner lätt kan förflytta sig genom deras strukturer. fasta elektrolyter är önskvärda i många konsumentprodukter, eftersom de inte läcker.
Litiumtinnfosfor-sulfid, Li10SnP2S12, är en fast elektrolyt för användning i litiumjonbatterier. den fasta elektrolytens kristallstruktur i kombination med dess svaga växelverkan med litiumjoner ger en miljö som litiumjoner lätt kan hoppa igenom.
4. Elektrolyter har enorm betydelse för de elektrokemiska processerna i levande organismer.De viktigaste jonerna i dessa elektrolyter är kalcium (Ca2+), magnesium (Mg2+), natrium (Na+), kalium (K+), klorid (Cl-), vätekarbonat (HCO3-) och vätefosfat (HPO42-).
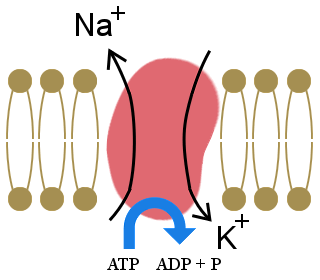
The importance of the sodium-potassium pump, shown in the diagram, to our lives is illustrated by the fact that it uses one-third of our resting energy.The pump maintains our cells’ electrolyte balance, with excess potassium ions inside cells and excess sodium ions outside cells.
This concentration gradient creates a voltage across the cell wall, which allows electrical signals to be transmitted in neurons and in muscles.It also provides the energy for processes in cell-membranes.
