Documento técnico de Robert L. Wilbur, Pharm.D., CPh | Director Ejecutivo, Asuntos Médicos, Gensco Pharma
Resumen
Los medicamentos tópicos se utilizan ampliamente como tratamientos de prescripción o de venta libre (OTC) para una variedad de condiciones. Aunque su uso es común, existe una importante confusión entre el público en general y algunos profesionales con formación médica, en cuanto a la diferencia entre productos tópicos y transdérmicos. Mientras que todos los compuestos tópicos y transdérmicos se aplican sobre la piel, sólo las fórmulas transdérmicas están diseñadas para penetrar a través de la capa cutánea y ejercer sus efectos sobre tejidos más profundos o distantes. Los productos transdérmicos utilizan varios métodos para mejorar la penetración a través del estrato córneo, la barrera primaria de la piel, permitiendo que cantidades suficientes del fármaco lleguen a la circulación sistémica o a los tejidos subyacentes más profundos. Los compuestos tópicos sólo penetran mínimamente en la capa de la piel, que es su intención de diseño. La utilización de la vía transdérmica permite un tratamiento específico para cada lugar, eliminando o minimizando los problemas de comorbilidades, reacciones adversas a los fármacos, interacción entre fármacos y efectos secundarios, lo que da lugar a complicaciones gastrointestinales, hepáticas, renales o de otro tipo.
Introducción
Los compuestos se han aplicado en la piel durante miles de años para mejorar la belleza y tratar afecciones locales. Sin embargo, la mayoría de los compuestos y/o fármacos aplicados tópicamente se absorben mal, si es que lo hacen. Esto se debe al tamaño y la polaridad de la molécula del fármaco y al efecto barrera de la piel. Muchos compuestos están destinados a permanecer en la superficie de la piel (tópicos), como los protectores solares, los repelentes de insectos y los antisépticos, mientras que otros penetran en las capas de la piel (transdérmicos) para dirigirse a sitios dentro de la piel o justo debajo de ella.
Más recientemente, la tecnología de administración transdérmica se ha desarrollado para tratar una serie de afecciones más allá del lugar de aplicación local. La administración transdérmica puede ofrecer ventajas significativas con respecto a la administración oral debido a que el metabolismo de primer paso es mínimo, se evita el entorno gastrointestinal adverso y se puede proporcionar una administración prolongada y controlada del fármaco. Algunos ejemplos son la lidocaína, la colchicina, la escopolamina, el estradiol y la testosterona, la nitroglicerina y el fentanilo. A pesar de estas ventajas, la mayoría de los principios activos no pueden administrarse por vía transdérmica debido a su tamaño y estructura molecular.
Discusión
Los términos tópico y transdérmico se confunden a menudo, se utilizan indistintamente y se entienden mal. Esto se debe al hecho de que todos los medicamentos aplicados a la piel son tópicos por definición (aplicados en la parte superior de la piel). Sin embargo, el término medicamento tópico se refiere generalmente a los medicamentos aplicados a la piel que se basan en la difusión pasiva en la propia piel, creando un efecto local. Mientras que los medicamentos transdérmicos se refieren a los medicamentos que se aplican a la piel pero que implican compuestos o tecnología de mejora de la penetración cutánea que aumentan la cantidad de fármaco que puede atravesar la barrera cutánea, a menudo hasta el punto de que el fármaco puede entrar en la circulación sistémica y ejercer efectos en zonas distintas del lugar de aplicación.
Para entender mejor esta diferencia, es importante comprender la piel y su función de barrera. La piel es el órgano más grande del cuerpo humano y representa aproximadamente el 10% de la masa corporal. La función principal de la piel es servir de barrera entre el cuerpo y el entorno exterior. Esta barrera protege contra la radiación UV, los microorganismos, los alérgenos y las sustancias químicas, así como contra la pérdida de agua y nutrientes. Además, la piel participa en muchas otras funciones, como la regulación térmica, el metabolismo y el control de la presión arterial. La piel también es un importante órgano sensorial que proporciona información sobre el entorno, como la temperatura, la presión y la estimulación nociva (dolor).
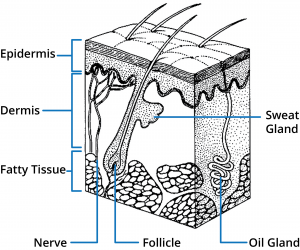 La piel humana está compuesta por tres regiones principales: epidermis, dermis y tejidos subcutáneos. Hay una serie de apéndices asociados a la piel, como los folículos pilosos y las glándulas sudoríparas ecrinas y apocrinas. Desde el punto de vista de la permeabilidad de la piel, la capa más externa de la epidermis, el estrato córneo, constituye la principal barrera y, por lo tanto, comprender esta estructura es fundamental para diseñar sistemas óptimos de administración tópica y transdérmica de fármacos.
La piel humana está compuesta por tres regiones principales: epidermis, dermis y tejidos subcutáneos. Hay una serie de apéndices asociados a la piel, como los folículos pilosos y las glándulas sudoríparas ecrinas y apocrinas. Desde el punto de vista de la permeabilidad de la piel, la capa más externa de la epidermis, el estrato córneo, constituye la principal barrera y, por lo tanto, comprender esta estructura es fundamental para diseñar sistemas óptimos de administración tópica y transdérmica de fármacos.
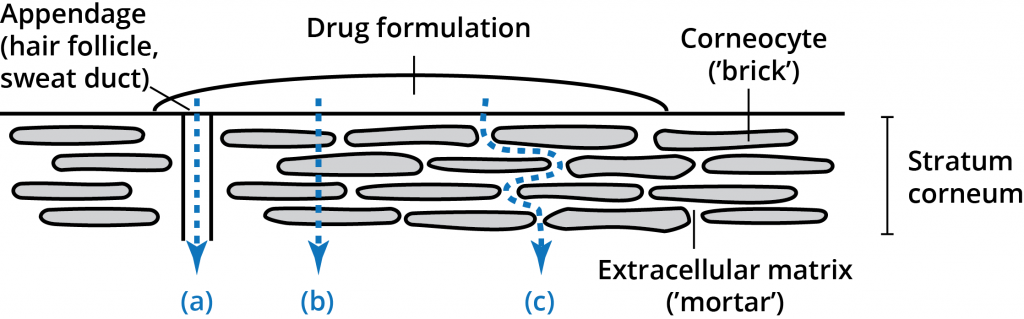
La capa del estrato córneo (la capa córnea) está formada por 10-20 micrómetros de capas celulares de alta densidad y baja hidratación. Aunque esta capa sólo tiene una profundidad de 10-15 células, es la principal barrera. La capa córnea se ha descrito como una estructura similar a una pared de ladrillos, con los corneocitos como «ladrillos» en una matriz (el «mortero») de lípidos intercelulares. La composición única de los lípidos intercelulares del estrato córneo y su disposición estructural en múltiples capas laminares dentro de un dominio lipídico continuo es fundamental para la función de barrera del estrato córneo. Un permeante aplicado a la piel tiene tres posibles rutas a través de la epidermis: a través de los apéndices (a), a través de los corneocitos (b – ruta transcelular), y a través de las capas de la matriz (c – ruta intercelular). Estas vías no son mutuamente excluyentes, ya que la mayoría de los compuestos permean la piel a través de una combinación de vías basada en las propiedades fisicoquímicas de la molécula permeante.
 Aunque las bicapas lipídicas intercelulares ocupan sólo una pequeña área del estrato córneo, proporcionan la única vía continua a través del estrato córneo. Muchos años de investigación han demostrado la importancia de esta ruta para la permeación de fármacos a través del estrato córneo. Tanto las moléculas lipídicas como las polares pueden ser transportadas a través de esta ruta intercelular, pero la cantidad y la velocidad de difusión dependen en gran medida de las propiedades fisicoquímicas del permeante.
Aunque las bicapas lipídicas intercelulares ocupan sólo una pequeña área del estrato córneo, proporcionan la única vía continua a través del estrato córneo. Muchos años de investigación han demostrado la importancia de esta ruta para la permeación de fármacos a través del estrato córneo. Tanto las moléculas lipídicas como las polares pueden ser transportadas a través de esta ruta intercelular, pero la cantidad y la velocidad de difusión dependen en gran medida de las propiedades fisicoquímicas del permeante.
El proceso de permeación implica una serie de procesos que comienzan con la liberación del permeante (el fármaco) de la forma farmacéutica (vehículo), seguido de la difusión en y a través del estrato córneo, luego la partición en el entorno epidérmico más acuoso y la difusión en tejidos más profundos o la absorción por la circulación cutánea. Estos procesos dependen en gran medida de la solubilidad y la difusividad del permeante en cada entorno. Debido a esta amplia variabilidad en la permeabilidad de diversas moléculas de fármacos, se han desarrollado varias estrategias para facilitar la permeabilidad de los fármacos a través de la epidermis. Los métodos de mejora física (microagujas, sonoforesis, iontoforesis, microabrasiones) no son pertinentes para este debate, ya que alteran activamente la estructura de la piel. La mejora de la difusión pasiva puede lograrse mediante dos métodos principales: El aumento de la actividad termodinámica del fármaco en las formulaciones (sobresaturaciones), y el uso de potenciadores de la penetración química (CPE) que interactúan con los componentes de la piel para promover el flujo del fármaco. Mientras que la sobresaturación está todavía en fase experimental, los CPEs se han utilizado ampliamente durante décadas.
Los CPEs son compuestos farmacológicamente inactivos que difunden y dividen la piel e interactúan reversiblemente con los componentes del estrato córneo, específicamente las bicapas lipídicas intercelulares. Es probable que las sustancias que perturban las disposiciones altamente ordenadas de las bicapas lipídicas intercelulares reduzcan la resistencia a la difusión del estrato córneo a la mayoría de las moléculas farmacológicas. El efecto es el desarrollo de poros o canales en las bicapas lipídicas a través de los cuales pueden pasar las moléculas de fármacos. Hay cientos de sustancias CPE disponibles para la formulación de un vehículo de administración de fármacos, cuya selección se basa en las propiedades fisicoquímicas de la molécula permeante, la forma de aplicación y el riesgo de daño cutáneo. La selección y formulación adecuadas de uno o más CPE con un fármaco específico puede aumentar la absorción transdérmica del fármaco desde el 1-5% del fármaco aplicado, como se observa con la aplicación tópica sin CPE, hasta tasas superiores al 40%. El aumento del fármaco que atraviesa la piel, el flujo, permite una penetración tisular más profunda del fármaco y su captación por la circulación cutánea proporcionando una actividad sistémica.
Hasta la fecha, la mayoría de los sistemas de administración transdérmica de productos farmacéuticos han sido parches. Los parches, por sí mismos, no mejoran la capacidad de las moléculas de los fármacos para penetrar en la piel, pero pueden aumentar la absorción del fármaco debido a los prolongados tiempos de aplicación. La matriz de formulación del parche, o reservorio, mantiene el gradiente de concentración del fármaco dentro del dispositivo después de la aplicación, de modo que el suministro del fármaco a la interfaz entre el parche y la piel es sostenido. La alta concentración de fármaco y la naturaleza oclusiva del parche pueden hacer que cantidades modestas de fármaco atraviesen la piel con el tiempo, aunque la mayor parte del fármaco aplicado permanece en el parche. Los continuos avances en el desarrollo de compuestos y tecnología CPE, como los sistemas de administración de nanopartículas, incluidas las micelas, están abriendo la vía de administración transdérmica a fármacos nuevos y antiguos por igual. Las micelas son moléculas lipídicas que se disponen en forma esférica en soluciones acuosas. La formación de una micela responde a la naturaleza anfipática de los ácidos grasos, lo que significa que contienen tanto regiones hidrofílicas (grupos de cabeza polares) como regiones hidrofóbicas (la larga cadena hidrofóbica). Las micelas contienen grupos de cabeza polares que suelen formar el exterior como la superficie de las micelas. Están orientados hacia el agua porque son polares. Las colas hidrofóbicas están en el interior y alejadas del agua ya que son no polares. Las micelas pueden secuestrar moléculas de fármacos lipofílicos dentro de la esfera y permitir el movimiento de estas moléculas a través de entornos polares. El sistema transdérmico creado por Gensco Pharma utiliza un vehículo formador de micelas que encapsula el fármaco y se combina con los CPE para aumentar aún más la cantidad y la velocidad de permeación. El aumento del flujo permite que una mayor cantidad del permeante atraviese la barrera cutánea más rápidamente y esté disponible para los tejidos más profundos y la circulación cutánea que los sistemas típicos de parches. Ahora se está evaluando la posibilidad de administrar por vía transdérmica medicamentos que son eficaces para determinadas afecciones pero cuyo uso estaba limitado por sus efectos gastrointestinales adversos, su elevado metabolismo de primer paso y su escasa biodisponibilidad. La administración controlada y sostenida de fármacos mediante el diseño de nanopartículas y el uso de la piel como reservorio de fármacos está revolucionando la forma de ver la administración transdérmica de medicamentos. Ahora podemos decir realmente que tenemos piel en el juego de los fármacos.
Conclusión
Los continuos avances en la mejora de la penetración de la piel están permitiendo la administración transdérmica de fármacos nuevos y antiguos, proporcionando efectos terapéuticos prolongados y una mayor seguridad para el paciente. Comprender las diferencias de formulación y penetración entre los medicamentos tópicos y transdérmicos es crucial para seleccionar el producto adecuado para un uso específico. Los medicamentos destinados a ejercer efectos clínicos en zonas tisulares distantes o más profundas requieren un vehículo transdérmico especialmente diseñado. Estos vehículos (geles, parches, películas, etc.) suelen incluir uno o más potenciadores de la penetración química para aumentar la penetración transdérmica y lograr el resultado deseado. Sin embargo, el clínico debe saber que no todos los parches o geles tópicos son transdérmicos. La mayoría de las cremas, los geles, las pomadas y los parches son meras formulaciones tópicas con una penetración limitada, o nula, del fármaco en los tejidos y la circulación por debajo de la piel. Comprender las diferencias entre los medicamentos transdérmicos (LiDORx, ColciGel, SpeedGel, Trans-Scop, Androgel, etc.) y los preparados tópicos (parches de lidocaína, cremas, cremas de esteroides, cremas para hongos, antibióticos y la mayoría de los productos tópicos de venta libre) permitirá seleccionar adecuadamente la mejor opción para el paciente.
Washington C, Washington N. Drug delivery to the skin. En: Physiological Pharmaceutics, Biological Barriers to drug absorption. 1st Ed Ellis Horwood 1989:109-120
Marjukka Suhonen TA, Bouwstra J. Chemical enhancement of percutaneous absorption in relation to stratum corneum structural alterations. J Control Release 1999:59:149-161
Ellias PM. Epidermal lipids, membranes, and keratinization. Int J Dermatol 1981:20:1-19
Michaels AS, Shaw JE. Drug permeation through human skin: Teoría y medición experimental in vitro. AIChE J 1975:21:985-996
Barry BW. Lipid protein partition theory of skin penetration enhancement. J Control Release 1991:15:237-248
Roberts MS. Targeted drug delivery to the skin and deeper tissues; The role of physiology, solute structure, and disease. Clin Exp Pharmacol Physiol 1997:24:874-9
Scheuplein RJ. Permeabilidad de la piel. Physiol Rev 1971:51:702-747
Mitragotri S. Breaking the skin barrier. Adv Drug Deliv Rev 2004:56:555-716
Barry BW. Novel mechanisms and devices to enable successful transdermal drug delivery. Eur J Pharm Sci 2001:14:101-114
Garavito MR. Detergentes como herramientas en la bioquímica de membranas. J Biol Chm 2001:276:32403-6