Ferroceno contendo agroquímicos
A proteção das culturas é uma questão importante na agricultura, possibilitada, em parte, pela utilização de produtos químicos para controle de pragas ou como herbicidas. Por outro lado, a crescente preocupação com os efeitos adversos dos pesticidas na saúde e no meio ambiente, evidenciada pela introdução de novos procedimentos de registro de pesticidas (ver, por exemplo, a Food Quality Protection Act nos Estados Unidos), motivou a investigação de novos pesticidas, incluindo pesticidas naturais à base de produtos, para substituir os compostos que não poderiam mais ser utilizados, devido aos novos requisitos de registro. Exemplos podem ser encontrados em várias revisões . Na tentativa de obter compostos mais eficientes, o grupo ferrocenil foi introduzido como substituto em compostos conhecidos como ativos.
Importantes agentes sistêmicos com amplo espectro de atividade fungicida contra patógenos vegetais são derivados do 1H-1,2,4-triazol, como os mostrados na Figura 2.

Exemplos de agroquímicos à base de 1H-1,2,4-triazol.
Por isso, não é surpreendente que a maioria dos agroquímicos à base de ferrocene (fungicidas, herbicidas) contenha o mesmo heterociclo. Além disso, muitas vezes os mesmos compostos revelaram uma actividade reguladora do crescimento das plantas promissora e algo inesperada. A síntese é bastante simples, começando pelo acetilferroceno, 1, ou ferrocenocarbaldeído, 2, e usando reações orgânicas clássicas, como ilustrado nas Figuras 3 e 4.

Strategies for the synthesis of 1H-1,2,4-triazole based ferrocenyl agrochemicals, starting from acetylferrocene.

Strategies for the synthesis of 1H-1,2,4-triazole based ferrocenyl agrochemicals, starting from ferrocenecarbaldehyde.
E and Z isomers of 3-aryl-1-ferrocenyl-2-triazolyl derivatives, 3, were tested for preventive fungicidal activity against powdery mildew on barley (foliar and soil drench applications) and for curative fungicidal activity against brown rust on wheat (foliar application). Selected results from foliar applications are reported in Table 1 (entry 1). Os isômeros E apresentaram melhor atividade fungicida do que os Z, provavelmente devido a uma característica estéril favorável. Além disso, foi detectada atividade reguladora do crescimento das plantas, pulverizando folhas de maçã de plantas cultivadas a partir de sementes. Reagindo ambos os isômeros com fenilidrazina (Figura 3), foram obtidos 5-aril-3-ferrocenil-1-fenil-4-triazolildihidropyrazoles, 4, que foram testados contra algumas cepas bacterianas, com resultados não muito satisfatórios.
O anel triazolil foi distanciado do ferroceno inserindo outro átomo de carbono , e os derivados (E)-3-aril-1-ferrocenil-2-triazolilmetilo, 5, (Figura 3) resultantes foram testados contra alguns fungos (Pratylenchus zeae, Alternaria solani, Cladosporium fulvum, Physalospora piricola e Cercospora arachidicola), com atividades variáveis, geralmente melhores contra A. solani (Tabela 1, entrada 2). Os derivados da reação com fenilidrazina, 6, desta vez, apresentaram um melhor desempenho (Tabela 1, entrada 3).
Ferrocenil análogos de triadimefon, 7, foram testados para atividades antifúngicas contra míldio e ferrugem em plantas de trigo intravital (Isariopsis clavispora, Bremia lactucae, C. fulvum, Erysiphe graminis e Alternaria mali), mas, decepcionantemente, todos os compostos testados mostraram menor atividade antifúngica (ver exemplos na Tabela 1, entrada 4) contra todos os fungos do que o triadimefon dos pais (92,8% e 96,6%, respectivamente). Ao invés disso, a atividade regulatória da planta, testada pelo método de rizogênese de cotilédones de pepino, resultou excelente.
Ao reduzir os análogos de triadimefon, foram obtidos os correspondentes análogos de ferrocenil do triadimenol, 8. Eles foram testados como indicado acima para os análogos de triadimefon e geralmente não apresentaram nenhuma atividade antifúngica (Tabela 1, entrada 5); entretanto, todos eles mostraram excelente capacidade reguladora do crescimento da planta, ainda maior do que os precursores de keto.
Uma leve variação estrutural foi a mudança de OH para OMe, 9 . Foram utilizados cinco fungos (P. zeae, A. solani, C. fulvum, P. piricola, e C. ara), com resultados modestos (ver, para exemplos seleccionados, Tabela 1, entrada 6). Resultados interessantes foram obtidos a partir da atividade reguladora do crescimento de plantas, determinada pelo alongamento de gemas de trigo e métodos de rootagem de cotilédones de pepino.
Uma abordagem diferente para sintetizar derivados do ferroceno contendo triazol foi partir do ferrocenocarbaldeído e α-bromo arylketones que permitiram variações estruturais (Figura 4) .
As três famílias de compostos (com CO, 11, OH, 12, e OMe, 13, funcionalidades, respectivamente) foram testadas para atividades biológicas. Foi observada uma escassa atividade reguladora do crescimento das plantas (testes de coleópteros de trigo e cotilédones de pepino), um pouco menos com cetonas. Foi registrada alguma atividade antifúngica in vitro (vs. Gibberella zeae, A. solani, Cercospora arachidicola, P. piricola, Phomopsis asparagi, Cladosporium cucumerinum, Sclerotinia sclerotiorum, e Pyricularia oryzae), mas não foi significativa, segundo os autores, se comparada com agentes comerciais conhecidos. Alguns dados selecionados são mostrados na Tabela 1 (entradas 8 a 10).
Ferrocenil derivados com diferentes funcionalidades também foram investigados. Vale ressaltar que uma das primeiras tentativas de ter os ferrocenos biologicamente ativos introduziu as hidrazinas aromáticas como substituintes (Figura 5 ): mais de uma década depois, foi reconhecida a importância dos compostos naturais contendo hidrazina, também com relação às atividades biológicas .

Synthesis of N-tert-butyl-N,N’-diacylhydrazines .
N-tert-butyl-N,N′-diacylhydrazines, mimicking the action of 20-hydroxyecdysone to activate the ecdysone receptor, lead to lethal premature molting, thus constituting a class of insect growth regulators useful in crop protection. The larvicidal activities were tested against Southern armyworm by foliar application. Results (Figure 6) indicate a good larvicidal activity, in comparison with the reference RH5849 (N-tert-butyl-N,N′-dibenzoylhydrazine) only when the tert-butyl group was far from ferrocenyl moiety.

Larvicidal activities (%) of N-tert-butyl-N,N’-diacylhydrazines with ferrocenoyl as one of the acyl groups .
1,1′-Disubstitued ferrocenes with different keto-ester, hydroxy-ester, and dihydroxy functionalities on both cyclopentadienyl rings were prepared (Figure 7 ) and assayed in vitro for antifungal activity against G. zeae, A. solani, C. arachidicola, P. piricola, and Fusarium oxysporum. The compounds showed relatively low fungicidal activity.

Example of synthesis of aroyl 1,1′-disubstituted ferrocenes .
Instead, ferrocenyl ethers , much easier to prepare (Figure 8) than previous diferrocenyl derivatives, showed moderate activity against two plant fungi, Botrytis cinerea and Penicillium species (Table 2).

Synthesis of ferrocenyl ethers 17-19.
Among herbicides, it is important to mention a series of cyanoacrylates containing ferrocene (Figure 9 ), that exhibited, according to the authors, excellent herbicidal activities against rape weeds.

Synthesis of ferrocenyl cyanoacrylates .
More recently, a series of ferrocenes substituted with pyrimidines (17 to 20, Figure 10) were prepared , because of their potentialities as herbicides and plant growth regulators, but the biological activities have not been tested yet. O mesmo vale para o trifluorometilsulfanilferroceno, 21, (trifluorometilsulfanil)etinylferroceno, 22, e (N-ferrocenilmetil)benzenocarbamida, 23, mostrado na Figura 10.

estruturas de derivados ferrocenílicos contendo pirimidina ou SCF3 , com possível atividade biológica.
Ferrocenos como catalisadores na síntese de agroquímicos
A importância dos agroquímicos é evidente, embora as conseqüências ambientais do seu uso não devem ser subestimadas. Portanto, é importante limitar a quantidade de produtos químicos introduzidos no meio ambiente. Além disso, tornou-se cada vez mais evidente que as propriedades biológicas dos agroquímicos quirais estão relacionadas com a configuração absoluta. O enantiômero não ativo é desnecessário ou até mesmo nocivo, de modo que a síntese enantioselectiva se tornou uma obrigação. O problema é bem ilustrado pelo caso do (S)-metolacloro (Figura 11, IUPAC: (S)-N-(2-etil-6-metil)fenil-N-(1-metil-2-metoxi)etil-2-cloroetanamida), o herbicida mais importante da Divisão de Proteção de Cultivos da Novartis (>20,000 ton/ano).

Ligantes ferrocenílicos quirais como catalisadores na síntese enantioselectiva do herbicida (S)-metolacloroetanamida.
É produzido desde 1978, primeiro como uma mistura racémica, depois (a partir de 1997) como forma enantiomericamente enriquecida, que permitiu uma redução de 40% da carga ambiental. Uma das estratégias mais importantes de síntese assimétrica é o uso de catalisadores quirais. O ponto de viragem para a síntese assimétrica do metolacloro foi o uso de um catalisador iridium , feito quiral por um ligante ferrocenilposfano quiral, Josiphos. O catalisador era suficientemente robusto para assegurar um número de rotação (TON) e frequência de rotação (TOF) muito elevados.
Para o leitor não familiarizado com os ferrocenos, basta dizer que dois substituintes diferentes no mesmo anel ciclopentadienil dão origem a dois enantiómeros, que apresentam uma quiralidade planar (Figura 12). Cada enantiômero é indicado como R p ou S p (onde p significa planar), de acordo com as regras de Schlögl: o observador olha ao longo do eixo C 5 do ferroceno a partir do lado do anel Cp mais altamente substituído, e a configuração absoluta é dada dependendo do arco mais curto a descer em prioridade, seja no sentido horário ou anti-horário.

Origin of planar chirality in ferrocenes (top) (Reimpresso com permissão da Organometallics 32:5668-5704. Copyright (2013) American Chemical Society) e a regra de Schlögl para identificação de enantiômeros (inferior).
O sucesso de Josiphos e sua modificação de Xilifos impulsionou tanto as aplicações industriais de catalisadores quirais e a síntese de novos ferrocênios quirais quanto seu uso em síntese assimétrica . Assim, o primeiro Josifos foi o composto pai de uma família de ligantes quirais eficazes que encontraram aplicação na síntese enantioselectiva de outros compostos úteis na agricultura. Para dar apenas um exemplo, o aliado assimétrico do terciário α-fluoroketones, moléculas úteis para aplicações em drogas, agroquímicos e materiais funcionais, foi realizado, entre outros, com catalisadores ferrocenílicos quirais (Figura 13, ). Infelizmente, e.e.s são muito baixos para serem úteis.

alação enantioselectiva de α-fluoroketones para agroquímicos, com catalisadores quirais ferrocenílicos .
Ferrocenos na remediação do solo
Argilas nativas surgiram como um componente ativo dos solos que influenciam a sorção de cátions, ânions e produtos químicos orgânicos hidrofóbicos. Portanto, sua importância na remoção e retenção de poluentes está aumentando, também porque os íons de ferro dentro da malha argilosa participam de reações redox, que podem ser úteis contra a poluição por íons metálicos; por exemplo, pesquisadores do site de Hanford em Washington poderiam diminuir a quantidade de Cr(VI) no suprimento de água de 1 ppm para abaixo dos limites de detecção (7 a 8 ppb) reduzindo-a para o Cr(III) menos tóxico e menos solúvel, aproveitando o ferro estrutural argiloso, anteriormente reduzido a Fe(II) .
Para a remediação de solos contaminados, a aplicação de surfactantes está ganhando importância . Os tensioactivos à base de ferroceno têm a vantagem de actuar tanto como tensioactivos como como compostos redoxactivos. Portanto, uma série de tensoativos ferrocenílicos de diferentes comprimentos de cadeia foi empregada como intercalantes, a fim de determinar as condições quando a transferência eletrônica ocorre em Fe estruturais argilosos. Através desta investigação, foi possível obter um melhor conhecimento geral da atividade do Fe em silicatos naturais. Os tensoativos ferrocenílicos (25 e 26 na figura 14a) utilizados como intercalantes, com diferentes comprimentos de cadeia, asseguraram uma gama de potenciais e uma gama de conformações possíveis; como argila, montmorilonita padrão Wyoming (SWy-1), de fórmula (Al2.88Fe0.68Mg0.47)(Si7.7Al0.29)O20(OH)4, foi utilizado.

Sais de ferrocenilamónio utilizados em estudos relativos à remediação do solo (a) ref. 52 , (b) ref. 53.
The results indicated that ferrocenyl trimethylammonium derivatives with C6 (25) and C11 (26) chains can be oxidized by structural Fe(III) in clay, whereas ferrocenylmethyl trimethylammonium (24) is not oxidized (Figure 15).

Energy scheme for redox reactions of ferrocenyl surfactants with structural Fe(III) in clay .
Later, other ferrocenyl surfactants (27 and 28 in Figure 14b) were used to verify the possibility to exploit them as reversible surfactants . In fact, although the surfactant washing of contaminated soils and groundwater may be an effective approach, operating costs result high and the surfactants need to be recycled, in order to optimize surfactant-enhanced remediation (SER). As discussed in ref. , the methods developed are not satisfactory. Deste estudo resultou que a solubilização do benzeno, tolueno e etilbenzeno com tensoactivos ferrocenílicos foi melhor do que a dos tensoactivos catiónicos (brometo de hexadeciltrimetilamónio (CTABr)) ou aniónicos (sulfato de sódio e dodecilo (SDS)). Além disso, a eficiência de remoção foi maior em baixas concentrações de tensoativos ferrocenílicos e, finalmente, a oxidação ao cátion ferrocênico permitiu a separação dos compostos orgânicos e, portanto, a reciclagem do tensoativo.
Vale a pena mencionar que os ferrocenos se mostraram úteis para evidenciar as propriedades redox do Fe(II) adsorvido em superfícies minerais. A medição de potenciais significativos de repouso em sistemas ambientais e geoquímicos tem sido muito difícil no passado, devido, entre outros fatores, à lenta transferência de elétrons entre o eletrodo de detecção sólido (tipicamente Pt) e as espécies ativas redox. Em vez disso, a abordagem de transferência de elétrons mediada por ferroceno gerou sondas de solução móvel que podem reagir com as espécies ativas redox suficientemente rápido para fornecer uma corrente mensurável, fornecendo assim uma medida direta da reatividade redox (ou seja, taxas de transferência de elétrons) das espécies ativas redox adsorvidas.
Ferrocenos como sensores
Derivados do ferroceno podem funcionar tanto como sensores ópticos quanto eletroquímicos. Quando oportunamente substituídos, eles podem coordenar ânions ou cátions, com uma conseqüente mudança potencial de mudança ou de cor. Apenas exemplos recentes selecionados serão relatados aqui.
- a)
Compostos neutros. Hidrazina e derivados são usados na agricultura como pesticidas, mas entram no meio ambiente também por emissões industriais. Devido ao seu risco toxicológico, são necessários métodos analíticos sensíveis, confiáveis e rápidos. Várias técnicas instrumentais estão disponíveis, mas as electroanalíticas podem fornecer procedimentos portáteis, baratos e rápidos, apesar de um pouco cinético, a oxidação da hidrazina é lenta. Explorando nanotubos de carbono, a determinação eletrocatalítica da fenilidrazina e hidrazina foi realizada contemporaneamente, com um eletrodo de pasta de nanotubos de carbono modificado com ferrocênio. Tal eletrodo resultou estável e de fácil preparação e renovação superficial. Ele mostrou uma seletividade melhorada e permitiu a detecção de hidrazina e fenilidrazina na mesma amostra, contemporaneamente.
- b)
Aniões. A importância do aspartato é inegável: como muitos ânions quirais, ele entra em processos biológicos e químicos, para não falar do aspartame de importância industrial. Por outro lado, o reconhecimento enantioselectivo por moléculas hospedeiras artificiais é de crescente interesse. Um número de 1.1′ – ferrocenos desubstituídos, com um átomo de carbono quiral e uma tiourea nos substitutos, foram preparados, e seu reconhecimento enantioselectivo foi testado. Pelo menos dois deles apresentaram bom reconhecimento quiral, como demonstrado pela titulação óptica com L- ou D-N-acetilasparato em solução de dimetil sulfóxido (DMSO). As mudanças de cor são significativas, como ilustrado na Figura 16, tornando estes sensores colorimétricos a olho nu.
Figure 16 
sensor colorimétrico à base de ferroceno para N-acetilasparato. Da esquerda para a direita: derivado ferrocenílico acima, o mesmo + L-N-acetilasparato, o mesmo + D-N-acetilasparato; derivado ferrocenílico abaixo, o mesmo + L-N-acetilasparato, o mesmo + D-N-acetilasparato. Adaptado de Ref. Eur J Org Chem 841-849. Reproduzido com permissão. Copyright (2009) Wiley.
- c)
Cations. A detecção de cátions de metais pesados no ambiente é de grande importância, devido à sua difusão a partir de fontes industriais e ao seu tratamento para a saúde. Em particular, o envenenamento por chumbo ainda é uma das doenças ambientais mais comuns e a detecção de íons Pb(II) é absolutamente necessária, especialmente na água potável. Após o reconhecimento dos ânions relacionados ao fosfato por uma ferrocenilimidazofenantrolina, que funcionava tanto como sensor colorimétrico quanto eletroquímico, os mesmos autores prepararam ferrocenos substituídos por imidazopiridina (ImPy) ou imidazofenazina (ImPhen) (Figura 17), que atuavam como receptores seletivos para os cátions Pb(II).
Figure 17 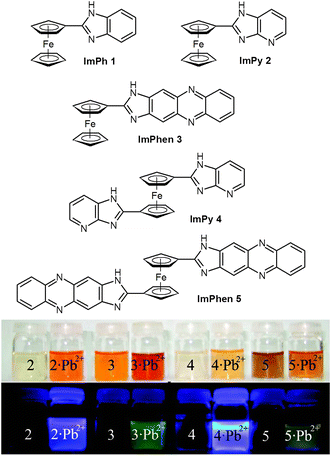
Sondas multicanais seletivas para cátions Pb(II); alterações de cor associadas à complexação catiônica (acima, absorção, abaixo, emissão). Adaptado de Ref. J Org Chem 74:4787-4796, reimpresso com permissão. Copyright (2009) American Chemical Society.
The compounds, reported in Figure 17, show highly selective affinity for Pb(II) ions over a range of other metal ions, through different channels, i.e., as redox, chromogenic, and fluorescent chemosensors. For example, compound ImP2 showed, upon complexation with Pb(II) cation, an oxidation redox peak anodically shifted (ΔE 1/2 = 150 mV), a red-shifted absorption maximum (Δλ = 44 nm) and an emission with an important chelation-enhanced fluorescence effect.

Ferrocenyl thiourea as electrochemical chemodosimeter for Hg(II) cation .
Outros quimiossensores à base de ferroceno, um selectivo para catiões Hg(II) e outro selectivo para catiões Cu(II), foram desenvolvidos introduzindo 1,4-benzenodiamina 31, 4,4′-bifenildiamina 32, ou 4,4′-diaminobenzenodissulfureto, 33 . Os compostos resultaram em quimiossensores colorométricos altamente sensíveis para Cu(II) e Hg(II), com alterações que permitiram a detecção a olho nu, como pode ser visto na Figura 19.

