White Paper by Robert L. Wilbur, Pharm.D., CPh | Executive Director, Medical Affairs, Gensco Pharma
Abstract
Leki miejscowe są szeroko stosowane jako leki na receptę lub bez recepty (OTC) w leczeniu różnych schorzeń. Chociaż ich stosowanie jest powszechne, wśród ogółu społeczeństwa i niektórych specjalistów medycznych panuje duże zamieszanie co do różnicy między produktami miejscowymi i transdermalnymi. Podczas gdy wszystkie związki miejscowe i transdermalne są stosowane na skórę, tylko preparaty transdermalne są zaprojektowane tak, aby przenikać przez warstwę skóry i wywierać swoje działanie na głębsze lub bardziej odległe tkanki. Produkty transdermalne wykorzystują kilka metod zwiększających penetrację przez warstwę rogową naskórka, stanowiącą podstawową barierę skóry, dzięki czemu wystarczająca ilość leku dociera do krążenia ogólnoustrojowego lub głębiej położonych tkanek. Związki stosowane miejscowo tylko w minimalnym stopniu przenikają przez warstwę skóry, co jest ich przeznaczeniem. Wykorzystanie drogi transdermalnej umożliwia leczenie specyficzne dla danego miejsca, eliminując lub minimalizując problemy związane z chorobami współistniejącymi, niepożądanymi reakcjami na leki, interakcjami lek/lek oraz działaniami niepożądanymi, skutkującymi powikłaniami żołądkowo-jelitowymi, wątrobowymi, nerkowymi lub innymi.
Wprowadzenie
Związki są stosowane na skórę od tysięcy lat w celu poprawy urody i leczenia miejscowych schorzeń. Jednak większość związków i/lub leków stosowanych miejscowo jest słabo wchłaniana, jeśli w ogóle. Wynika to z wielkości i polarności cząsteczki leku oraz bariery ochronnej, jaką stanowi skóra. Wiele związków ma pozostawać na powierzchni skóry (miejscowo), jak np. filtry przeciwsłoneczne, środki odstraszające owady i antyseptyczne, podczas gdy inne przenikają do warstw skóry (transdermalnie), aby dotrzeć do miejsc docelowych w skórze lub tuż pod nią.
Ostatnio technologia transdermalnego dostarczania leków została opracowana w celu leczenia wielu schorzeń poza miejscowym miejscem aplikacji. Podawanie transdermalne może oferować znaczące korzyści w porównaniu z podawaniem doustnym ze względu na minimalny metabolizm pierwszego przejścia, unikanie niekorzystnego środowiska przewodu pokarmowego oraz możliwość zapewnienia długotrwałego i kontrolowanego dostarczania leku. Przykłady obejmują lidokainę, kolchicynę, skopolaminę, estradiol i testosteron, nitroglicerynę i fentanyl. Pomimo tych zalet, większość aktywnych składników nie może być dostarczana transdermalnie ze względu na ich rozmiar i strukturę molekularną.
Dyskusja
Pojęcia miejscowe i transdermalne są często mylone, używane zamiennie i słabo rozumiane. Wynika to z faktu, że wszystkie leki stosowane na skórę są z definicji lekami miejscowymi (stosowanymi na wierzchnią warstwę skóry). Jednak termin leki miejscowe odnosi się ogólnie do leków nakładanych na skórę, które opierają się na biernej dyfuzji do samej skóry, tworząc efekt miejscowy. Natomiast leki transdermalne odnoszą się do leków, które są stosowane na skórę, ale zawierają związki zwiększające penetrację skóry lub technologię, która zwiększa ilość leku, który może przekroczyć barierę skórną, często do punktu, w którym lek może dostać się do krążenia ogólnoustrojowego i wywierać wpływ w obszarach innych niż miejsce aplikacji.
Aby lepiej zrozumieć tę różnicę, ważne jest zrozumienie skóry i jej funkcji barierowej. Skóra jest największym organem ludzkiego ciała, stanowiącym około 10% masy ciała. Podstawową funkcją skóry jest tworzenie bariery między ciałem a środowiskiem zewnętrznym. Bariera ta chroni przed promieniowaniem UV, mikroorganizmami, alergenami, substancjami chemicznymi oraz utratą wody i składników odżywczych. Ponadto, skóra pełni wiele innych funkcji, takich jak regulacja termiczna, metabolizm i kontrola ciśnienia krwi. Skóra jest również ważnym narządem zmysłów, dostarczającym informacji o środowisku, takich jak temperatura, ciśnienie i szkodliwa stymulacja (ból).
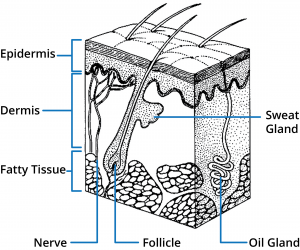 Skóra człowieka składa się z trzech głównych regionów: naskórka, skóry właściwej i tkanki podskórnej. Ze skórą związana jest pewna liczba przydatków, w tym mieszki włosowe oraz gruczoły potowe ekrynowe i apokrynowe. Z punktu widzenia przenikania przez skórę, najbardziej zewnętrzna warstwa naskórka, warstwa rogowa, stanowi główną barierę i dlatego zrozumienie tej struktury ma fundamentalne znaczenie dla projektowania optymalnych systemów miejscowego i transdermalnego dostarczania leków.
Skóra człowieka składa się z trzech głównych regionów: naskórka, skóry właściwej i tkanki podskórnej. Ze skórą związana jest pewna liczba przydatków, w tym mieszki włosowe oraz gruczoły potowe ekrynowe i apokrynowe. Z punktu widzenia przenikania przez skórę, najbardziej zewnętrzna warstwa naskórka, warstwa rogowa, stanowi główną barierę i dlatego zrozumienie tej struktury ma fundamentalne znaczenie dla projektowania optymalnych systemów miejscowego i transdermalnego dostarczania leków.
Warstwa rogowa (warstwa rogowa) składa się z 10-20 mikrometrów warstw komórek o dużej gęstości i niskim uwodnieniu. Mimo że warstwa ta ma głębokość zaledwie 10-15 komórek, stanowi podstawową barierę. Warstwa rogowa jest opisywana jako struktura przypominająca mur z cegieł, w której korneocyty są „cegłami” w matrycy („zaprawie”) lipidów międzykomórkowych. Unikalny skład lipidów międzykomórkowych warstwy rogowej i ich ułożenie w wielu warstwach płytkowych w ciągłej domenie lipidowej ma decydujące znaczenie dla funkcji barierowej warstwy rogowej. Substancja przenikająca przez skórę ma trzy możliwe drogi przejścia przez naskórek: przez przydatki (a), przez korneocyty (b – droga transkomórkowa) i przez warstwy macierzy (c – droga międzykomórkowa). Ścieżki te nie wykluczają się wzajemnie, większość związków przenika przez skórę kombinacją ścieżek w zależności od właściwości fizykochemicznych przenikającej cząsteczki.
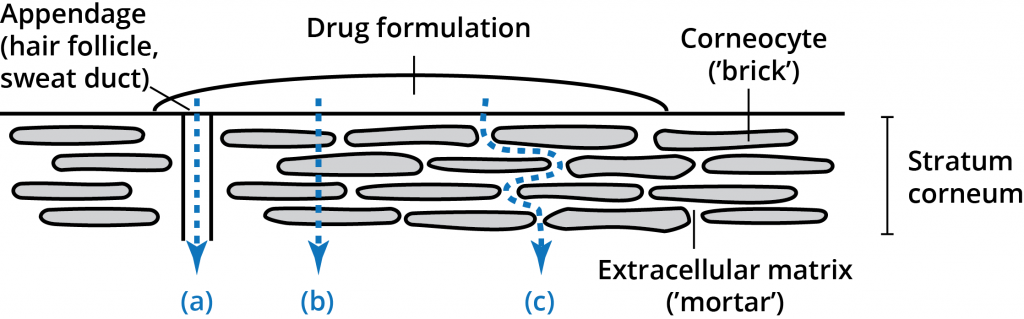 Pomimo, że międzykomórkowe warstwy lipidowe zajmują tylko niewielką powierzchnię warstwy rogowej, stanowią jedyną ciągłą drogę przez warstwę rogową. Wieloletnie badania wykazały znaczenie i wagę tej drogi dla przenikania leków przez warstwę rogową naskórka. Zarówno cząsteczki lipidowe, jak i polarne mogą być transportowane tą drogą międzykomórkową, ale ilość i szybkość dyfuzji zależą w dużym stopniu od właściwości fizykochemicznych substancji przenikającej.
Pomimo, że międzykomórkowe warstwy lipidowe zajmują tylko niewielką powierzchnię warstwy rogowej, stanowią jedyną ciągłą drogę przez warstwę rogową. Wieloletnie badania wykazały znaczenie i wagę tej drogi dla przenikania leków przez warstwę rogową naskórka. Zarówno cząsteczki lipidowe, jak i polarne mogą być transportowane tą drogą międzykomórkową, ale ilość i szybkość dyfuzji zależą w dużym stopniu od właściwości fizykochemicznych substancji przenikającej.
Proces przenikania obejmuje szereg procesów, począwszy od uwolnienia substancji przenikającej (leku) z postaci leku (nośnika), poprzez dyfuzję do i przez warstwę rogową naskórka, a następnie podział do bardziej wodnistego środowiska naskórka i dyfuzję do głębszych tkanek lub wychwyt przez krążenie skórne. Procesy te w dużym stopniu zależą od rozpuszczalności i dyfuzyjności permeantu w każdym z tych środowisk. Ze względu na tak dużą zmienność w przenikalności różnych cząsteczek leków, opracowano kilka strategii ułatwiających przenikanie leków przez naskórek. Fizyczne metody zwiększania przenikania (mikroigły, sonoforeza, jonoforeza, mikrootarcia) nie są istotne w tej dyskusji, ponieważ aktywnie zaburzają strukturę skóry. Zwiększenie dyfuzji biernej można osiągnąć za pomocą dwóch podstawowych metod: Zwiększenie aktywności termodynamicznej leku w preparatach (przesycenie) oraz zastosowanie chemicznych środków wspomagających penetrację (CPE), które oddziałując ze składnikami skóry, zwiększają strumień leku. Podczas gdy przesycanie jest nadal w fazie eksperymentalnej, CPE są szeroko stosowane od dziesięcioleci.
CPE są farmakologicznie nieaktywnymi związkami, które dyfundują i dzielą skórę oraz odwracalnie oddziałują ze składnikami warstwy rogowej naskórka, a w szczególności z międzykomórkowymi dwuwarstwami lipidowymi. Substancje, które zaburzają wysoce uporządkowany układ międzykomórkowych dwuwarstw lipidowych, prawdopodobnie zmniejszają opór dyfuzyjny warstwy rogowej naskórka dla większości cząsteczek leków. Efektem tego jest powstanie porów lub kanałów w dwuwarstwach lipidowych, przez które mogą przenikać cząsteczki leku. Istnieją setki substancji CPE dostępnych do formulacji nośnika leku, których wybór jest oparty na właściwościach fizykochemicznych cząsteczki permeantu, sposobie aplikacji i ryzyku uszkodzenia skóry. Właściwy dobór i formulacja jednego lub więcej CPE z określonym lekiem może zwiększyć transdermalne wchłanianie leku z 1-5% zaaplikowanego leku, jak to obserwuje się w przypadku miejscowej aplikacji bez CPE, do wskaźników przekraczających 40%. Zwiększenie ilości leku przenikającego przez skórę pozwala na głębszą penetrację tkanek przez lek i wchłanianie przez krążenie skórne, co zapewnia działanie ogólnoustrojowe.
Do tej pory większość systemów transdermalnego dostarczania leków stanowiły plastry. Plastry same w sobie nie zwiększają zdolności cząsteczek leku do przenikania przez skórę, ale mogą zwiększyć wchłanianie leku ze względu na wydłużony czas aplikacji. Formuła plastra, czyli rezerwuar, utrzymuje gradient stężenia leku w urządzeniu po aplikacji, dzięki czemu dostarczanie leku do miejsca styku plastra ze skórą jest utrzymane. Wysokie stężenie leku i okluzyjny charakter plastra mogą powodować przenikanie niewielkich ilości leku przez skórę w miarę upływu czasu, chociaż większość zaaplikowanego leku pozostaje w plastrze. Stałe postępy w rozwoju związków i technologii CPE, takich jak nanocząsteczkowe systemy dostarczania leku, w tym micele, otwierają transdermalną drogę podawania zarówno dla nowych, jak i starych leków. Micele to cząsteczki lipidów, które w roztworach wodnych układają się w formę kulistą. Tworzenie się miceli jest odpowiedzią na amfipatyczną naturę kwasów tłuszczowych, co oznacza, że zawierają one zarówno obszary hydrofilowe (polarne grupy główne), jak i hydrofobowe (długi łańcuch hydrofobowy). Micele zawierają polarne grupy nagłówkowe, które zwykle tworzą zewnętrzną część powierzchni miceli. Są one skierowane w stronę wody, ponieważ są polarne. Ogony hydrofobowe znajdują się wewnątrz i z dala od wody, ponieważ są niepolarne. Micele mogą sekwestrować lipofilowe cząsteczki leków w obrębie sfery i umożliwiać przemieszczanie się tych cząsteczek przez polarne środowiska. System transdermalny stworzony przez Gensco Pharma wykorzystuje nośnik tworzący micele, który kapsułkuje lek i łączy się z CPE w celu dalszego zwiększenia ilości i szybkości przenikania. Zwiększony strumień pozwala większej ilości permeantu szybciej przemieszczać się przez barierę skórną i być dostępnym do głębszych tkanek i krążenia skórnego niż w przypadku typowych systemów plastrów. Leki, które są skuteczne w określonych schorzeniach, ale ich stosowanie było ograniczone ze względu na niekorzystne efekty żołądkowo-jelitowe, wysoki metabolizm pierwszego przejścia i słabą biodostępność, są obecnie oceniane pod kątem podawania transdermalnego. Kontrolowane i trwałe dostarczanie leków poprzez projektowanie nanocząsteczek i wykorzystanie skóry jako rezerwuaru leku rewolucjonizuje sposób, w jaki patrzymy na transdermalne podawanie leków. Możemy teraz naprawdę powiedzieć, że mamy skórę w grze o leki.
Wniosek
Ciągłe postępy w zakresie poprawy penetracji skóry pozwalają na transdermalne podawanie nowych i starych leków, zapewniając przedłużone efekty terapeutyczne i zwiększone bezpieczeństwo pacjentów. Zrozumienie różnic w formule i przenikaniu między lekami stosowanymi miejscowo i transdermalnie jest kluczowe dla wyboru odpowiedniego produktu do konkretnego zastosowania. Leki, które mają wywierać działanie kliniczne w odległych lub głębiej położonych tkankach, wymagają specjalnie zaprojektowanego nośnika transdermalnego. Nośniki te (żele, plastry, folie itp.) często zawierają jeden lub więcej chemicznych środków zwiększających penetrację, aby zwiększyć penetrację transdermalną w celu osiągnięcia pożądanego efektu. Jednakże klinicysta powinien być świadomy, że nie wszystkie plastry lub żele miejscowe są transdermalne. Większość kremów, żeli, maści i plastrów to jedynie preparaty miejscowe o ograniczonym, jeśli w ogóle, przenikaniu leku do tkanek i krążenia pod skórą. Zrozumienie różnic między lekami transdermalnymi (LiDORx, ColciGel, SpeedGel, Trans-Scop, Androgel itp.) a preparatami stosowanymi miejscowo (plastry z lidokainą, kremy, kremy steroidowe, kremy przeciwgrzybicze, antybiotyki i większość produktów OTC stosowanych miejscowo) pozwoli na właściwy wybór najlepszej opcji dla pacjenta.
Washington C, Washington N. Drug delivery to the skin. In: Physiological Pharmaceutics, Biological Barriers to drug absorption. 1st Ed Ellis Horwood 1989:109-120
Marjukka Suhonen TA, Bouwstra J. Chemical enhancement of percutaneous absorption in relation to stratum corneum structural alterations. J Control Release 1999:59:149-161
Ellias PM. Epidermal lipids, membranes, and keratinization. Int J Dermatol 1981:20:1-19
Michaels AS, Shaw JE. Drug permeation through human skin: Theory and in vitro experimental measurement. AIChE J 1975:21:985-996
Barry BW. Lipid protein partition theory of skin penetration enhancement. J Control Release 1991:15:237-248
Roberts MS. Targeted drug delivery to the skin and deeper tissues; The role of physiology, solute structure, and disease. Clin Exp Pharmacol Physiol 1997:24:874-9
Scheuplein RJ. Permeability of the skin. Physiol Rev 1971:51:702-747
Mitragotri S. Breaking the skin barrier. Adv Drug Deliv Rev 2004:56:555-716
Barry BW. Novel mechanisms and devices to enable successful transdermal drug delivery. Eur J Pharm Sci 2001:14:101-114
Garavito MR. Detergents as tools in membrane biochemistry. J Biol Chm 2001:276:32403-6