White Paper by Robert L. Wilbur, Pharm.D., CPh | Executive Director, Medical Affairs, Gensco Pharma
Abstrakt
Topické léky jsou široce používány jako léčba na předpis nebo volně prodejné (OTC) pro různé stavy. Ačkoli je jejich používání běžné, mezi širokou veřejností a některými lékařsky vzdělanými odborníky panuje značný zmatek, pokud jde o rozdíl mezi topickými a transdermálními přípravky. Zatímco všechny lokální a transdermální přípravky se aplikují na kůži, pouze transdermální přípravky jsou navrženy tak, aby pronikaly vrstvou kůže a působily na hlubší nebo vzdálenější tkáně. Transdermální přípravky využívají několik metod pro zvýšení průniku přes stratum corneum, primární bariéru kůže, což umožňuje dostatečnému množství léčiva dostat se buď do systémového oběhu, nebo do hlubších podkožních tkání. Lokální sloučeniny pronikají vrstvou kůže jen minimálně, což je jejich zamýšlený záměr. Využití transdermální cesty umožňuje léčbu specifickou pro dané místo a eliminuje nebo minimalizuje problémy s komorbiditami, nežádoucími účinky léků, interakcemi mezi léky a vedlejšími účinky, které mají za následek gastrointestinální, jaterní, renální nebo jiné komplikace.
Úvod
Sloučeniny se na kůži aplikují již tisíce let za účelem zkrášlení a léčby lokálních onemocnění. Většina lokálně aplikovaných sloučenin a/nebo léčiv se však vstřebává špatně, pokud vůbec. Je to způsobeno velikostí a polaritou molekuly léčiva a bariérovým efektem kůže. Mnohé sloučeniny jsou určeny k tomu, aby zůstaly na povrchu kůže (topické), jako jsou opalovací krémy, repelenty proti hmyzu a antiseptika, zatímco jiné pronikají do vrstev kůže (transdermální) na cílová místa v kůži nebo těsně pod ní.
Nejnověji byla vyvinuta technologie transdermálního podávání k léčbě řady stavů mimo lokální místo aplikace. Transdermální podání může mít oproti perorálnímu podání významné výhody díky minimálnímu metabolismu při prvním průchodu, vyhnutí se nepříznivému gastrointestinálnímu prostředí a schopnosti zajistit dlouhodobé a kontrolované podávání léčiva. Příklady zahrnují lidokain, kolchicin, skopolamin, estradiol a testosteron, nitroglycerin a fentanyl. Navzdory těmto výhodám nelze většinu účinných látek podávat transdermálně vzhledem k jejich molekulární velikosti a struktuře.
Diskuse
Pojmy lokální a transdermální jsou často zaměňovány, používány zaměnitelně a špatně chápány. To vyplývá ze skutečnosti, že všechny léky aplikované na kůži jsou podle definice topické (aplikované na vrchní část kůže). Termín lokální léky však obecně označuje léky aplikované na kůži, které jsou závislé na pasivní difúzi do samotné kůže a vytvářejí lokální účinek. Zatímco transdermální léky označují léky, které se aplikují na kůži, ale zahrnují sloučeniny nebo technologie zvyšující penetraci kůží, které zvyšují množství léčiva, jež může projít kožní bariérou, často do té míry, že se léčivo může dostat do systémového oběhu a působit v jiných oblastech než v místě aplikace.
Pro lepší pochopení tohoto rozdílu je důležité porozumět kůži a její bariérové funkci. Kůže je největší orgán lidského těla, který tvoří zhruba 10 % tělesné hmotnosti. Primární funkcí kůže je funkce bariéry mezi tělem a vnějším prostředím. Tato bariéra chrání před UV zářením, mikroorganismy, alergeny a chemickými látkami a před ztrátou vody a živin. Kromě toho se kůže podílí i na mnoha dalších funkcích, jako je tepelná regulace, metabolismus a regulace krevního tlaku. Kůže je také důležitým smyslovým orgánem, který poskytuje informace o prostředí, jako je teplota, tlak a škodlivé podněty (bolest).
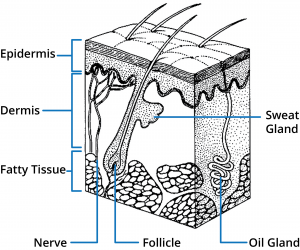 Lidská kůže se skládá ze tří hlavních oblastí: epidermis, dermis a podkoží. S kůží je spojena řada přídatných orgánů včetně vlasových folikulů a ekrinních a apokrinních potních žláz. Z hlediska prostupnosti kůží představuje nejsvrchnější vrstva epidermis, stratum corneum, hlavní bariéru, a proto je pochopení této struktury zásadní pro návrh optimálních systémů pro lokální a transdermální podávání léčiv.
Lidská kůže se skládá ze tří hlavních oblastí: epidermis, dermis a podkoží. S kůží je spojena řada přídatných orgánů včetně vlasových folikulů a ekrinních a apokrinních potních žláz. Z hlediska prostupnosti kůží představuje nejsvrchnější vrstva epidermis, stratum corneum, hlavní bariéru, a proto je pochopení této struktury zásadní pro návrh optimálních systémů pro lokální a transdermální podávání léčiv.
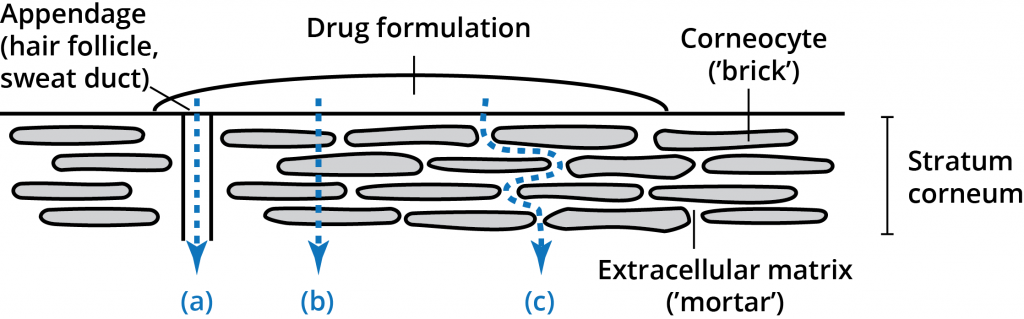
Vrstva stratum corneum (rohová vrstva) se skládá z 10-20 mikrometrů velkých vrstev buněk s vysokou hustotou a nízkou hydratací. Přestože je tato vrstva hluboká pouze 10-15 buněk, představuje primární bariéru. Vrstva stratum corneum byla popsána jako struktura podobná cihlové zdi s korneocyty jako „cihlami“ v matrici („maltě“) mezibuněčných lipidů. Jedinečné složení mezibuněčných lipidů stratum corneum a jejich strukturální uspořádání v několika lamelárních vrstvách v souvislé lipidové doméně je rozhodující pro bariérovou funkci stratum corneum. Permeant aplikovaný na kůži má tři možné cesty přes epidermis: přes přívěsky (a), přes korneocyty (b – transcelulární cesta) a přes matrixové vrstvy (c – mezibuněčná cesta). Tyto cesty se vzájemně nevylučují, většina sloučenin prostupuje kůží kombinací cest v závislosti na fyzikálně-chemických vlastnostech prostupující molekuly.
 Přestože mezibuněčné lipidové dvojvrstvy zabírají pouze malou plochu rohové vrstvy, představují jedinou souvislou cestu přes rohovou vrstvu. Mnohaletý výzkum prokázal význam a důležitost této cesty pro prostup léčiv přes stratum corneum. Touto mezibuněčnou cestou jsou schopny být transportovány jak lipidové, tak polární molekuly, ale množství a rychlost difuze jsou velmi závislé na fyzikálně-chemických vlastnostech permeantu.
Přestože mezibuněčné lipidové dvojvrstvy zabírají pouze malou plochu rohové vrstvy, představují jedinou souvislou cestu přes rohovou vrstvu. Mnohaletý výzkum prokázal význam a důležitost této cesty pro prostup léčiv přes stratum corneum. Touto mezibuněčnou cestou jsou schopny být transportovány jak lipidové, tak polární molekuly, ale množství a rychlost difuze jsou velmi závislé na fyzikálně-chemických vlastnostech permeantu.
Proces permeace zahrnuje řadu procesů, které začínají uvolněním permeantu (léčiva) z lékové formy (vehikula), následuje difuze do rohové vrstvy a skrz ni, poté rozdělení do vodnatějšího epidermálního prostředí a difuze do hlubších tkání nebo vychytávání kožním oběhem. Tyto procesy jsou vysoce závislé na rozpustnosti a difuzivitě permeantu v jednotlivých prostředích. Vzhledem k této velké variabilitě v permeabilitě různých molekul léčiv bylo vyvinuto několik strategií pro usnadnění prostupu léčiv přes epidermis. Fyzikální metody zesílení (mikrojehly, sonoforéza, iontoforéza, mikrooděrky) nejsou pro tuto diskusi relevantní, protože aktivně narušují strukturu kůže. Pasivního zvýšení difuze lze dosáhnout dvěma základními metodami: Zvýšení termodynamické aktivity léčiva ve formulacích (přesycení) a použití chemických zesilovačů penetrace (CPE), které interagují se složkami kůže a podporují tok léčiva. Zatímco supersaturace je stále ve fázi experimentů, CPE se široce používají již několik desetiletí.
CPE jsou farmakologicky neaktivní sloučeniny, které difundují a rozdělují kůži a reverzibilně interagují se složkami stratum corneum, konkrétně s mezibuněčnými lipidovými dvojvrstvami. Látky, které narušují vysoce uspořádané uspořádání mezibuněčných lipidových dvojvrstev, pravděpodobně snižují difuzní odolnost stratum corneum vůči většině molekul léčiv. Výsledkem je vznik pórů nebo kanálů v lipidových dvojvrstvách, kterými mohou molekuly léčiv procházet. Pro formulaci nosiče léčiva jsou k dispozici stovky CPE látek, jejichž výběr je založen na fyzikálně-chemických vlastnostech permeantní molekuly, způsobu aplikace a riziku poškození kůže. Správný výběr a formulace jedné nebo více CPE s určitým léčivem může zvýšit transdermální absorpci léčiva z 1-5 % aplikovaného léčiva, jak je tomu při lokální aplikaci bez CPE, na míru vyšší než 40 %. Zvýšení průchodu léčiva kůží, flux, umožňuje hlubší průnik léčiva do tkáně a absorpci kožním oběhem zajišťující systémovou aktivitu.
Dosud byla většina systémů transdermálního podání léčivých přípravků tvořena náplastmi. Náplasti samy o sobě nezvyšují schopnost molekul léčiva prostupovat kůží, ale mohou zvýšit absorpci léčiva díky prodloužené době aplikace. Složení matrice náplasti nebo rezervoáru udržuje po aplikaci gradient koncentrace léčiva v zařízení, takže dodávka léčiva na rozhraní mezi náplastí a kůží je trvalá. Vysoká koncentrace léčiva a okluzivní povaha náplasti mohou v průběhu času prohnat kůží mírné množství léčiva, ačkoli většina aplikovaného léčiva zůstává v náplasti. Pokračující pokroky ve vývoji CPE sloučenin a technologií, jako jsou systémy podávání nanočástic, včetně micel, otevírají transdermální cestu podání novým i starším léčivům. Micely jsou lipidové molekuly, které se ve vodných roztocích uspořádávají do sférické formy. Tvorba micel je reakcí na amfipatickou povahu mastných kyselin, což znamená, že obsahují jak hydrofilní oblasti (polární hlavové skupiny), tak hydrofobní oblasti (dlouhý hydrofobní řetězec). Micely obsahují polární hlavové skupiny, které obvykle tvoří vnější stranu jako povrch micel. Jsou obráceny k vodě, protože jsou polární. Hydrofobní ocásky jsou uvnitř a směrem od vody, protože jsou nepolární. Micely mohou sekvestrovat lipofilní molekuly léčiv uvnitř sféry a umožnit pohyb těchto molekul polárním prostředím. Transdermální systém vytvořený společností Gensco Pharma využívá vehikulum tvořící micely, které zapouzdřuje léčivo a kombinuje se s CPE pro další zvýšení množství a rychlosti prostupu. Zvýšený tok umožňuje, aby se větší množství permeantu pohybovalo přes kožní bariéru rychleji a bylo k dispozici hlubším tkáním a kožnímu oběhu než u typických náplasťových systémů. Léčiva, která jsou účinná u specifických stavů, ale jejichž použití bylo omezeno kvůli nežádoucím gastrointestinálním účinkům, vysokému metabolismu při prvním průchodu a špatné biologické dostupnosti, se nyní vyhodnocují pro transdermální podání. Řízené a trvalé podávání léčiv prostřednictvím designu nanočástic a využití kůže jako zásobníku léčiv přináší revoluci v pohledu na transdermální podávání léčiv. Nyní můžeme skutečně říci, že máme kůži ve hře o léky.
Závěr
Pokračující pokroky ve zlepšování penetrace kůží umožňují transdermální podávání nových i starších léků, které poskytují prodloužené terapeutické účinky a vyšší bezpečnost pacientů. Pochopení rozdílů ve složení a penetraci mezi lokálními a transdermálními léčivy je zásadní pro výběr vhodného přípravku pro konkrétní použití. Léčiva, která mají mít klinické účinky ve vzdálených nebo hlubších tkáňových místech, vyžadují účelově navržený transdermální nosič. Tyto nosiče (gely, náplasti, filmy atd.) často obsahují jeden nebo více chemických zesilovačů penetrace, které zvyšují transdermální penetraci k dosažení požadovaného výsledku. Lékař by si však měl být vědom, že ne všechny náplasti nebo lokální gely jsou transdermální. Většina krémů, gelů, mastí a náplastí jsou pouze lokální přípravky s omezeným, pokud vůbec nějakým průnikem léčiva do tkání a krevního oběhu pod kůží. Pochopení rozdílů mezi transdermálními léky (LiDORx, ColciGel, SpeedGel, Trans-Scop, Androgel atd.) a topickými přípravky (lidokainové náplasti, krémy, steroidní krémy, plísňové krémy, antibiotika a většina volně prodejných topických přípravků) umožní správný výběr nejlepší varianty pro pacienta.
Washington C, Washington N. Drug delivery to the skin. In: Dějiny kůže v České republice: Fyziologická farmacie, Biologické bariéry vstřebávání léčiv. 1st Ed Ellis Horwood 1989:109-120
Marjukka Suhonen TA, Bouwstra J. Chemical enhancement of percutaneous absorption in relation to stratum corneum structural alterations. J Control Release 1999:59:149-161
Ellias PM. Epidermální lipidy, membrány a keratinizace. Int J Dermatol 1981:20:1-19
Michaels AS, Shaw JE. Drug permeation through human skin (Průnik léčiv lidskou kůží): Theory and in vitro experimental measurement. AIChE J 1975:21:985-996
Barry BW. Teorie rozdělení lipidů a proteinů pro zvýšení penetrace kůží. J Control Release 1991:15:237-248
Roberts MS. Targeted drug delivery to the skin and deeper tissues; The role of physiology, solute structure, and disease (Cílené podávání léčiv do kůže a hlubších tkání; Úloha fyziologie, struktury rozpuštěných látek a nemoci). Clin Exp Pharmacol Physiol 1997:24:874-9
Scheuplein RJ. Permeabilita kůže. Physiol Rev 1971:51:702-747
Mitragotri S. Breaking the skin barrier. Adv Drug Deliv Rev 2004:56:555-716
Barry BW. Nové mechanismy a zařízení umožňující úspěšné transdermální podávání léčiv. Eur J Pharm Sci 2001:14:101-114
Garavito MR. Detergenty jako nástroje v membránové biochemii. J Biol Chm 2001:276:32403-6