White Paper door Robert L. Wilbur, Pharm.D., CPh | Executive Director, Medical Affairs, Gensco Pharma
Abstract
Topische medicijnen worden op grote schaal gebruikt als receptgeneesmiddel of als vrij verkrijgbare (OTC) behandeling voor een verscheidenheid aan aandoeningen. Hoewel ze vaak worden gebruikt, bestaat er bij het grote publiek en bij sommige medisch geschoolde beroepsbeoefenaren grote verwarring over het verschil tussen topische en transdermale producten. Hoewel alle lokale en transdermale verbindingen op de huid worden aangebracht, zijn alleen de transdermale formuleringen ontworpen om door de huidlaag heen te dringen en hun effecten op dieper gelegen of verder gelegen weefsels uit te oefenen. Transdermale producten maken gebruik van verschillende methoden om de penetratie door het Stratum Corneum, de primaire barrière van de huid, te verbeteren, waardoor voldoende hoeveelheden van het geneesmiddel in de systemische circulatie of in diepere onderliggende weefsels terechtkomen. Topische verbindingen dringen slechts minimaal door in de huidlaag, wat ook de bedoeling is. Door gebruik te maken van de transdermale route is een specifieke behandeling mogelijk, waardoor problemen met comorbiditeit, bijwerkingen, geneesmiddel/geneesmiddel interactie en bijwerkingen, resulterend in GI, lever, nier of andere complicaties, worden geëlimineerd of geminimaliseerd.
Inleiding
Samenstellingen worden al duizenden jaren op de huid aangebracht om de schoonheid te verbeteren en lokale aandoeningen te behandelen. De meeste plaatselijk aangebrachte verbindingen en/of geneesmiddelen worden echter slecht of helemaal niet geabsorbeerd. Dit is te wijten aan de grootte en polariteit van de medicijnmolecule en de barrièrewerking van de huid. Veel verbindingen zijn bedoeld om op het huidoppervlak te blijven (topisch), zoals zonnebrandmiddelen, insectenwerende middelen en antiseptica, terwijl andere in de huidlagen doordringen (transdermaal) om zich te richten op plaatsen in de huid of net daaronder.
Meer recentelijk is de transdermale toedieningstechnologie ontwikkeld voor de behandeling van een reeks aandoeningen die verder reiken dan de plaatselijke plaats van toepassing. Transdermale toediening biedt aanzienlijke voordelen ten opzichte van orale toediening, omdat het metabolisme in de eerste fase minimaal is, het ongunstige maagdarmkanaal wordt vermeden en het geneesmiddel langdurig en gecontroleerd kan worden toegediend. Voorbeelden zijn lidocaïne, colchicine, scopolamine, oestradiol en testosteron, nitroglycerine en fentanyl. Ondanks deze voordelen kunnen de meeste werkzame stoffen niet transdermaal worden toegediend vanwege hun moleculaire grootte en structuur.
Discussie
De termen topisch en transdermaal worden vaak verward, door elkaar gebruikt, en slecht begrepen. Dit komt doordat alle medicijnen die op de huid worden aangebracht per definitie topisch zijn (aangebracht op de bovenkant van de huid). De term topische medicatie verwijst echter in het algemeen naar op de huid aangebrachte medicatie die berust op passieve diffusie in de huid zelf, waardoor een plaatselijk effect ontstaat. Transdermale geneesmiddelen daarentegen verwijzen naar geneesmiddelen die op de huid worden aangebracht, maar waarbij gebruik wordt gemaakt van stoffen die de huidpenetratie verbeteren of van technologie die de hoeveelheid geneesmiddel die de huidbarrière kan passeren, verhoogt, vaak in die mate dat het geneesmiddel in de systemische circulatie kan komen en effecten kan hebben op andere gebieden dan de plaats waar het is aangebracht.
Om dit verschil beter te begrijpen, is het belangrijk de huid en haar barrièrefunctie te begrijpen. De huid is het grootste orgaan van het menselijk lichaam en maakt ongeveer 10% uit van de massa van het lichaam. De voornaamste functie van de huid is een barrière te vormen tussen het lichaam en de externe omgeving. Deze barrière beschermt tegen UV-straling, micro-organismen, allergenen en chemicaliën, en tegen het verlies van water en voedingsstoffen. Daarnaast is de huid ook betrokken bij tal van andere functies, zoals warmteregeling, metabolisme en bloeddrukregeling. De huid is ook een belangrijk zintuig dat informatie verstrekt over de omgeving, zoals temperatuur, druk en schadelijke prikkels (pijn).
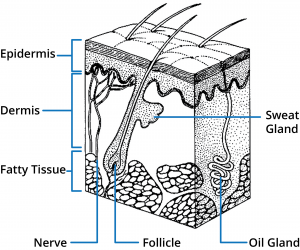 De menselijke huid bestaat uit drie hoofdregio’s: opperhuid, lederhuid en onderhuidse weefsels. Een aantal aanhangsels zijn verbonden met de huid, waaronder haarfollikels en eccriene en apocriene zweetklieren. Vanuit het oogpunt van huidpermeatie vormt de buitenste laag van de opperhuid, het stratum corneum, de belangrijkste barrière, en daarom is inzicht in deze structuur van fundamenteel belang voor het ontwerpen van optimale topische en transdermale medicijnafgiftesystemen.
De menselijke huid bestaat uit drie hoofdregio’s: opperhuid, lederhuid en onderhuidse weefsels. Een aantal aanhangsels zijn verbonden met de huid, waaronder haarfollikels en eccriene en apocriene zweetklieren. Vanuit het oogpunt van huidpermeatie vormt de buitenste laag van de opperhuid, het stratum corneum, de belangrijkste barrière, en daarom is inzicht in deze structuur van fundamenteel belang voor het ontwerpen van optimale topische en transdermale medicijnafgiftesystemen.
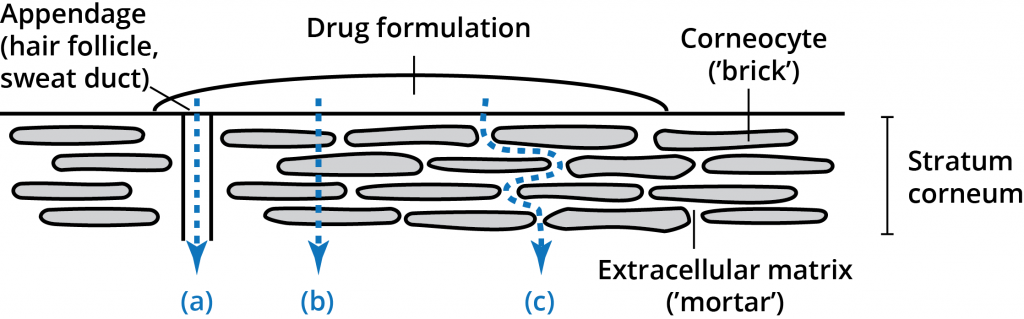
De stratum corneum laag (de hoornlaag) bestaat uit 10-20 micrometer cellagen met een hoge dichtheid en een lage hydratatie. Hoewel deze laag slechts 10-15 cellen diep is, vormt zij de primaire barrière. De hoornlaag is beschreven als een bakstenen muur-achtige structuur met corneocyten als de “stenen” in een matrix (de “mortel”) van intercellulaire lipiden. De unieke samenstelling van de intercellulaire lipiden van het stratum corneum en hun structurele rangschikking in meerdere lamellaire lagen binnen een continu lipidedomein is van cruciaal belang voor de barrièrefunctie van het stratum corneum. Een permeant die op de huid wordt aangebracht, kan drie routes door de epidermis volgen: door de aanhangsels (a), door de corneocyten (b – transcellulaire route), en door de matrixlagen (c – intercellulaire route). Deze routes sluiten elkaar niet uit; de meeste stoffen dringen door in de huid via een combinatie van routes, afhankelijk van de fysiochemische eigenschappen van het doordringende molecuul.
 Hoewel de intercellulaire lipidenbilagen slechts een klein deel van de hoornlaag beslaan, vormen zij de enige ononderbroken weg door de hoornlaag. Vele jaren van onderzoek hebben de betekenis en het belang van deze route voor de permeatie van geneesmiddelen door het stratum corneum aangetoond. Zowel lipide als polaire moleculen kunnen via deze intercellulaire route worden getransporteerd, maar de hoeveelheid en de snelheid van de diffusie zijn sterk afhankelijk van de fysiochemische eigenschappen van de permeant.
Hoewel de intercellulaire lipidenbilagen slechts een klein deel van de hoornlaag beslaan, vormen zij de enige ononderbroken weg door de hoornlaag. Vele jaren van onderzoek hebben de betekenis en het belang van deze route voor de permeatie van geneesmiddelen door het stratum corneum aangetoond. Zowel lipide als polaire moleculen kunnen via deze intercellulaire route worden getransporteerd, maar de hoeveelheid en de snelheid van de diffusie zijn sterk afhankelijk van de fysiochemische eigenschappen van de permeant.
Het permeatieproces omvat een reeks processen die beginnen met het vrijkomen van de permeant (het geneesmiddel) uit de doseringsvorm (het medium), gevolgd door de diffusie in en door het stratum corneum, vervolgens de partitionering in het meer waterige epidermale milieu en diffusie in diepere weefsels of opname door de cutane circulatie. Deze processen zijn sterk afhankelijk van de oplosbaarheid en diffusie van de permeant in elk milieu. Vanwege deze grote variabiliteit in permeabiliteit van verschillende geneesmiddelmoleculen zijn er verschillende strategieën ontwikkeld om de permeatie van geneesmiddelen door de epidermis te vergemakkelijken. Fysische methoden voor verbetering (micronaalden, sonoforese, iontoforese, microschaafwonden) zijn voor deze bespreking niet relevant, aangezien zij de huidstructuur actief verstoren. Passieve diffusieverbetering kan worden bereikt door twee primaire methoden: Het verhogen van de thermodynamische activiteit van het geneesmiddel in formuleringen (oververzadiging), en het gebruik van chemische penetratieverbeteraars (CPE’s) die interageren met huidbestanddelen om de geneesmiddelflux te bevorderen. Terwijl supersaturatie zich nog in de experimentele fase bevindt, worden CPE’s al tientallen jaren op grote schaal gebruikt.
CPE’s zijn farmacologisch inactieve verbindingen die diffunderen en de huid partitioneren en reversibel interageren met de stratum corneum componenten, met name de intercellulaire lipide bilayers. Stoffen die de sterk geordende rangschikking van de intercellulaire lipidebilagen verstoren, zullen waarschijnlijk de diffusieweerstand van het stratum corneum tegen de meeste geneesmiddelmoleculen verminderen. Het effect is de ontwikkeling van poriën of kanalen in de lipide bilagen waardoor de moleculen van het geneesmiddel kunnen passeren. Er zijn honderden CPE-stoffen beschikbaar voor de formulering van een medium voor de toediening van geneesmiddelen, waarvan de selectie is gebaseerd op de fysiochemische eigenschappen van de permeantmolecule, de wijze van toepassing en het risico van huidbeschadiging. De juiste selectie en formulering van een of meer CPE’s met een specifiek geneesmiddel kan de transdermale absorptie van het geneesmiddel verhogen van 1-5% van het aangebrachte geneesmiddel, zoals bij topische toepassing zonder CPE, tot percentages van meer dan 40%. De verbetering van de passage van het geneesmiddel door de huid, flux, maakt diepere weefselpenetratie van het geneesmiddel en opname door de huidcirculatie mogelijk, waardoor systemische activiteit ontstaat.
Tot op heden zijn de meeste transdermale afgiftesystemen voor geneesmiddelen patches geweest. Patches op zich verbeteren niet het vermogen van geneesmiddelenmoleculen om de huid door te dringen, maar kunnen de absorptie van geneesmiddelen verhogen door de langere aanbrengtijden. De formuleringsmatrix van de pleister, of het reservoir, handhaaft de concentratiegradiënt van het geneesmiddel in de pleister na het aanbrengen, zodat de afgifte van het geneesmiddel aan het raakvlak tussen de pleister en de huid wordt bestendigd. De hoge geneesmiddelconcentratie en de occlusieve aard van de pleister kunnen na verloop van tijd bescheiden hoeveelheden geneesmiddel door de huid drijven, hoewel het grootste deel van het aangebrachte geneesmiddel in de pleister blijft. Door de voortdurende vooruitgang in de ontwikkeling van CPE-verbindingen en -technologie, zoals systemen voor de toediening van nanodeeltjes, waaronder micellen, wordt de transdermale toedieningsroute opengesteld voor zowel nieuwe als oude geneesmiddelen. Micellen zijn lipidemoleculen die zich in een bolvorm ordenen in waterige oplossingen. De vorming van een micel is een reactie op de amfipathische aard van vetzuren, wat betekent dat zij zowel hydrofiele gebieden (polaire hoofdgroepen) als hydrofobe gebieden (de lange hydrofobe keten) bevatten. Micellen bevatten polaire hoofdgroepen die gewoonlijk de buitenkant vormen als het oppervlak van micellen. Zij zijn naar het water gericht omdat zij polair zijn. De hydrofobe staarten zitten binnenin en weg van het water omdat ze niet polair zijn. Micellen kunnen lipofiele geneesmiddelenmoleculen binnen de bol sekwestreren en de beweging van deze moleculen door polaire omgevingen mogelijk maken. Het transdermale systeem van Gensco Pharma maakt gebruik van een micelvormend vehikel dat het geneesmiddel inkapselt en combineert met CPE’s om de permeatiehoeveelheid en -snelheid verder op te voeren. De verhoogde flux zorgt ervoor dat een grotere hoeveelheid van het permeatiemiddel sneller door de huidbarrière kan dringen en beschikbaar is voor de diepere weefsels en de huidcirculatie dan bij typische patchsystemen. Geneesmiddelen die doeltreffend zijn voor specifieke aandoeningen, maar waarvan het gebruik beperkt was wegens ongunstige gastro-intestinale effecten, hoog first-pass metabolisme en slechte biologische beschikbaarheid, worden nu geëvalueerd voor transdermale toediening. Gecontroleerde en langdurige toediening van geneesmiddelen door het ontwerp van nanodeeltjes en door gebruik te maken van de huid als geneesmiddelreservoir betekent een revolutie in de manier waarop we naar transdermale toediening van geneesmiddelen kijken.
Conclusie
De voortdurende verbetering van de huidpenetratie maakt het mogelijk nieuwe en oude geneesmiddelen transdermaal toe te dienen, waardoor de therapeutische werking wordt verlengd en de veiligheid van de patiënt wordt verhoogd. Inzicht in de verschillen in formulering en penetratie tussen topische en transdermale geneesmiddelen is van cruciaal belang voor de keuze van het juiste product voor een specifiek gebruik. Geneesmiddelen die bedoeld zijn om klinische effecten uit te oefenen op verafgelegen of dieper gelegen weefsels vereisen een speciaal ontworpen transdermaal medium. Deze middelen (gels, pleisters, films, enz.) bevatten vaak een of meer chemische penetratieversterkers om de transdermale penetratie te verhogen en zo het gewenste resultaat te bereiken. De clinicus moet zich er echter van bewust zijn dat niet alle patches of topische gels transdermaal zijn. De meeste crèmes, gels, zalven en patches zijn slechts topische formuleringen met beperkte of geen penetratie van het geneesmiddel in de weefsels en de circulatie onder de huid. Inzicht in de verschillen tussen transdermale geneesmiddelen (LiDORx, ColciGel, SpeedGel, Trans-Scop, Androgel, enz.) en topische preparaten (lidocaïnepleisters, crèmes, steroïdencrèmes, schimmelcrèmes, antibiotica en de meeste OTC topische producten) zal het mogelijk maken de juiste keuze te maken voor de beste optie voor de patiënt.
Washington C, Washington N. Drug delivery to the skin. In: Physiological Pharmaceutics, Biological Barriers to drug absorption. 1st Ed Ellis Horwood 1989:109-120
Marjukka Suhonen TA, Bouwstra J. Chemical enhancement of percutaneous absorption in relation to stratum corneum structural alterations. J Control Release 1999:59:149-161
Ellias PM. Epidermale lipiden, membranen, en keratinisatie. Int J Dermatol 1981:20:1-19
Michaels AS, Shaw JE. Drug permeation through human skin: Theorie en in vitro experimentele metingen. AIChE J 1975:21:985-996
Barry BW. Lipid protein partition theory of skin penetration enhancement. J Control Release 1991:15:237-248
Roberts MS. Targeted drug delivery to the skin and deeper tissues; The role of physiology, solute structure, and disease. Clin Exp Pharmacol Physiol 1997:24:874-9
Scheuplein RJ. Permeabiliteit van de huid. Physiol Rev 1971:51:702-747
Mitragotri S. Breaking the skin barrier. Adv Drug Deliv Rev 2004:56:555-716
Barry BW. Novel mechanisms and devices to enable successful transdermal drug delivery. Eur J Pharm Sci 2001:14:101-114
Garavito MR. Detergenten als hulpmiddelen in membraan biochemie. J Biol Chm 2001:276:32403-6