White Paper av Robert L. Wilbur, Pharm.D., CPh | Executive Director, Medical Affairs, Gensco Pharma
Abstract
Topiska läkemedel används i stor utsträckning som receptbelagda eller receptfria (OTC) behandlingar för en mängd olika tillstånd. Även om användningen är vanlig finns det en betydande förvirring bland allmänheten och vissa medicinskt utbildade yrkesutövare när det gäller skillnaden mellan topiska och transdermala produkter. Alla topiska och transdermala föreningar appliceras på huden, men endast de transdermala formuleringarna är utformade för att tränga igenom hudskiktet och utöva sina effekter på djupare eller mer avlägsna vävnader. Transdermala produkter använder flera metoder för att öka penetrationen genom Stratum Corneum, hudens primära barriär, så att tillräckliga mängder av läkemedlet antingen når den systemiska cirkulationen eller djupare underliggande vävnader. Topiska preparat tränger endast minimalt in i hudskiktet, vilket är deras avsedda syfte. Användning av den transdermala vägen ger möjlighet till platsspecifik behandling, vilket eliminerar eller minimerar problem med komorbiditeter, biverkningar, läkemedelsinteraktioner och biverkningar som leder till gastrointestinala komplikationer, lever- och njurkomplikationer eller andra komplikationer.
Introduktion
Sammansättningar har applicerats på huden i tusentals år för att förbättra skönheten och behandla lokala tillstånd. De flesta topiskt applicerade föreningar och/eller läkemedel absorberas dock dåligt eller inte alls. Detta beror på läkemedelsmolekylens storlek och polaritet och hudens barriäreffekt. Många föreningar är avsedda att ligga kvar på hudytan (topiska), t.ex. solskyddsmedel, insektsmedel och antiseptiska medel, medan andra tränger in i hudlagren (transdermala) för att nå målpunkter i huden eller strax under den.
På senare tid har tekniken för transdermal tillförsel utvecklats för att behandla en rad olika tillstånd utanför den lokala applikationsstället. Transdermal tillförsel kan erbjuda betydande fördelar jämfört med oral administrering på grund av minimal förstapassmetabolism, undvikande av den ogynnsamma gastrointestinala miljön och förmågan att ge långvarig och kontrollerad läkemedelstillförsel. Som exempel kan nämnas lidokain, kolchicin, scopolamin, östradiol och testosteron, nitroglycerin och fentanyl. Trots dessa fördelar kan de flesta aktiva ingredienser inte levereras transdermalt på grund av deras molekylära storlek och struktur.
Diskussion
Tillhörningarna topiska och transdermala förväxlas ofta, används synonymt och är dåligt förstådda. Detta beror på att alla läkemedel som appliceras på huden per definition är topiska (appliceras på ovansidan av huden). Termen topisk medicinering avser dock i allmänhet läkemedel som appliceras på huden och som bygger på passiv diffusion i själva huden, vilket skapar en lokal effekt. Medan transdermala läkemedel hänvisar till läkemedel som appliceras på huden men som innefattar hudpenetrationsförbättrande föreningar eller teknik som ökar mängden läkemedel som kan passera hudbarriären, ofta till den grad att läkemedlet kan komma in i den systemiska cirkulationen och utöva effekter på andra områden än applikationsstället.
För att bättre förstå denna skillnad är det viktigt att förstå huden och dess barriärfunktion. Huden är det största organet i människokroppen och utgör ungefär 10 % av kroppens massa. Hudens primära funktion är att vara en barriär mellan kroppen och den yttre miljön. Barriären skyddar mot UV-strålning, mikroorganismer, allergener och kemikalier samt förlust av vatten och näringsämnen. Dessutom är huden också involverad i många andra funktioner, t.ex. värmereglering, ämnesomsättning och blodtryckskontroll. Huden är också ett viktigt sensoriskt organ som ger information om omgivningen, t.ex. temperatur, tryck och skadlig stimulering (smärta).
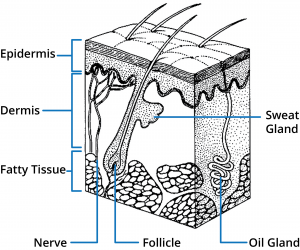 Människans hud består av tre huvudregioner: epidermis, dermis och subkutan vävnad. Ett antal bilagor är knutna till huden, bland annat hårsäckar och eckrina och apokrina svettkörtlar. Ur en hudpermeationssynpunkt utgör det yttersta lagret av epidermis, stratum corneum, den viktigaste barriären och därför är det grundläggande att förstå denna struktur för att utforma optimala topiska och transdermala system för läkemedelstillförsel.
Människans hud består av tre huvudregioner: epidermis, dermis och subkutan vävnad. Ett antal bilagor är knutna till huden, bland annat hårsäckar och eckrina och apokrina svettkörtlar. Ur en hudpermeationssynpunkt utgör det yttersta lagret av epidermis, stratum corneum, den viktigaste barriären och därför är det grundläggande att förstå denna struktur för att utforma optimala topiska och transdermala system för läkemedelstillförsel.
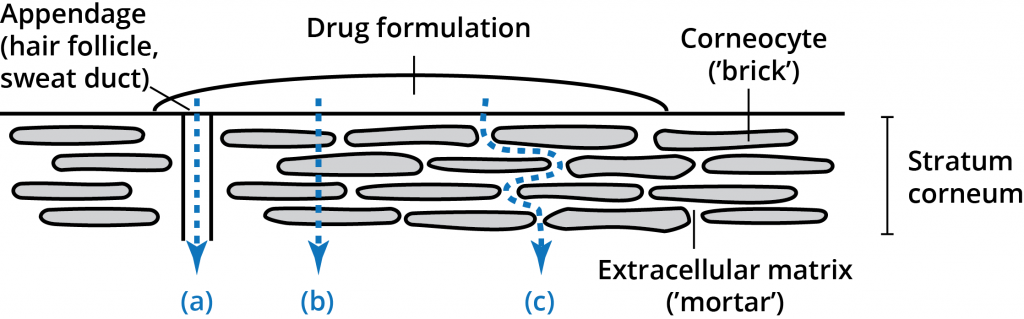
Stratum corneum-skiktet (det horniga lagret) består av 10-20 mikrometer cellskikt med hög densitet och låg hydrering. Även om detta lager bara är 10-15 celler djupt är det den primära barriären. Stratum corneum-skiktet har beskrivits som en tegelväggsliknande struktur med korneocyter som ”tegelstenar” i en matris (”murbruk”) av intercellulära lipider. Den unika sammansättningen av de intercellulära lipiderna i stratum corneum och deras strukturella arrangemang i flera lamellära lager inom en kontinuerlig lipiddomän är avgörande för stratum corneum:s barriärfunktion. En permeant som appliceras på huden har tre möjliga vägar genom epidermis: genom bilagorna (a), genom korneocyterna (b – transcellulär väg) och genom matrislagren (c – intercellulär väg). Dessa vägar utesluter inte varandra, och de flesta föreningar tränger igenom huden genom en kombination av vägar baserat på de fysiokemiska egenskaperna hos den genomträngande molekylen.
 Samtidigt som de intercellulära lipidbildelagren upptar endast en liten del av hornlagret, utgör de den enda kontinuerliga vägen genom hornlagret. Många års forskning har visat på betydelsen och vikten av denna väg för permeation av läkemedel genom stratum corneum. Både lipidmolekyler och polära molekyler kan transporteras genom denna intercellulära väg, men mängden och hastigheten av diffusionen är starkt beroende av permeationsmedlets fysiokemiska egenskaper.
Samtidigt som de intercellulära lipidbildelagren upptar endast en liten del av hornlagret, utgör de den enda kontinuerliga vägen genom hornlagret. Många års forskning har visat på betydelsen och vikten av denna väg för permeation av läkemedel genom stratum corneum. Både lipidmolekyler och polära molekyler kan transporteras genom denna intercellulära väg, men mängden och hastigheten av diffusionen är starkt beroende av permeationsmedlets fysiokemiska egenskaper.
Permeationsprocessen inbegriper en rad processer som börjar med frigörandet av permeationsmedlet (läkemedlet) från doseringsformen (vehikel), följt av diffusionen in i och genom hornlagret, sedan fördelning i den mer vattenhaltiga epidermala miljön och diffusion i djupare vävnader eller upptag i den kutana cirkulationen. Dessa processer är starkt beroende av permeationsmedlets löslighet och diffusionsförmåga i varje miljö. På grund av den stora variationen i permeabiliteten hos olika läkemedelsmolekyler har flera strategier utvecklats för att underlätta permeationen av läkemedel genom epidermis. Fysiska förbättringsmetoder (mikronålar, sonofores, jontofores, mikroslipning) är inte relevanta för den här diskussionen eftersom de aktivt stör hudens struktur. Passiv diffusionsförbättring kan uppnås med två primära metoder: Ökad termodynamisk aktivitet hos läkemedlet i formuleringar (övermättnad) och användning av kemiska penetrationsförstärkare (CPE) som interagerar med hudens beståndsdelar för att främja läkemedelsflödet. Medan övermättnad fortfarande befinner sig i försöksfasen har CPEs använts i stor utsträckning i årtionden.
CPEs är farmakologiskt inaktiva föreningar som diffunderar och delar upp huden och interagerar reversibelt med stratum corneum-komponenterna, särskilt de intercellulära lipidbilayers. Ämnen som stör de intercellulära lipidbilayers mycket välordnade arrangemang kommer sannolikt att minska stratum corneums diffusionsmotstånd mot de flesta läkemedelsmolekyler. Effekten är att det bildas porer eller kanaler i lipidbilayers genom vilka läkemedelsmolekylerna kan passera. Det finns hundratals CPE-substanser tillgängliga för formulering av en läkemedelsleverantör, och valet av dessa baseras på den permeanta molekylens fysiokemiska egenskaper, appliceringssättet och risken för hudskador. Rätt val och formulering av en eller flera CPEs med ett specifikt läkemedel kan öka den transdermala absorptionen av läkemedlet från 1-5 % av det applicerade läkemedlet, som vid topisk applicering utan CPE, till mer än 40 %. Den ökade mängden läkemedel som passerar genom huden möjliggör djupare vävnadspenetration av läkemedlet och upptag i den kutana cirkulationen, vilket ger systemisk aktivitet.
Hittills har de flesta transdermala leveranssystem för läkemedel varit plåster. Plåster förbättrar inte i sig själva läkemedelsmolekylernas förmåga att tränga igenom huden, men kan öka läkemedelsabsorptionen på grund av förlängd appliceringstid. Formuleringsmatrisen i plåstret, eller reservoaren, upprätthåller koncentrationen av läkemedel i anordningen efter applicering så att läkemedelstillförseln till gränssnittet mellan plåstret och huden bibehålls. Plåstrets höga läkemedelskoncentration och ocklusiva karaktär kan driva blygsamma mängder läkemedel genom huden med tiden, även om det mesta av det applicerade läkemedlet stannar kvar i plåstret. De pågående framstegen i utvecklingen av CPE-föreningar och teknik, t.ex. nanopartikelsystem, inklusive miceller, öppnar den transdermala administreringsvägen för både nya och gamla läkemedel. Miceller är lipidmolekyler som arrangerar sig i sfärisk form i vattenlösningar. Bildandet av en micell är ett svar på fettsyrornas amfipatiska natur, vilket innebär att de innehåller både hydrofila områden (polära huvudgrupper) och hydrofoba områden (den långa hydrofoba kedjan). Miceller innehåller polära huvudgrupper som vanligen utgör utsidan som micellernas yta. De vetter mot vattnet eftersom de är polära. De hydrofoba svansarna är på insidan och bort från vattnet eftersom de är opolära. Micellerna kan binda in lipofila läkemedelsmolekyler i sfären och göra det möjligt för dessa molekyler att röra sig genom polära miljöer. Det transdermala system som skapats av Gensco Pharma använder ett micellbildande vehikel som kapslar in läkemedlet och kombinerar det med CPE:er för att ytterligare öka mängden och hastigheten av permeation. Det ökade flödet gör det möjligt för en större mängd av permeationsmedlet att snabbare passera hudbarriären och bli tillgängligt för de djupare vävnaderna och den kutana cirkulationen än vad som är fallet med typiska plåstersystem. Läkemedel som är effektiva för specifika tillstånd men som begränsats i användningen på grund av negativa gastrointestinala effekter, hög förstapassmetabolism och dålig biotillgänglighet utvärderas nu för transdermal administrering. Kontrollerad och hållbar läkemedelstillförsel genom nanopartikeldesign och genom att använda huden som en läkemedelsreservoar revolutionerar vårt sätt att se på transdermal läkemedelstillförsel. Vi kan nu verkligen säga att vi har hud i läkemedelsspelet.
Slutsats
Fortsatta framsteg inom förbättrad hudpenetration gör det möjligt att administrera nya och gamla läkemedel transdermalt, vilket ger långvariga terapeutiska effekter och förbättrad patientsäkerhet. Att förstå formulerings- och penetrationsskillnaderna mellan topiska och transdermala läkemedel är avgörande för att kunna välja lämplig produkt för en specifik användning. Läkemedel som är avsedda att utöva kliniska effekter på avlägsna eller djupare vävnadsställen kräver en specialdesignad transdermal substans. Dessa medel (geler, plåster, filmer osv.) innehåller ofta en eller flera kemiska penetrationsförstärkare för att öka den transdermala penetrationen för att uppnå det önskade resultatet. Klinikern bör dock vara medveten om att inte alla plåster eller topiska geler är transdermala. De flesta krämer, geler, salvor och plåster är endast topiska formuleringar med begränsad, om ens någon, läkemedelsgenomträngning till vävnaderna och cirkulationen under huden. Om man förstår skillnaderna mellan transdermala läkemedel (LiDORx, ColciGel, SpeedGel, Trans-Scop, Androgel etc.) och topiska preparat (lidokainplåster, krämer, steroidkrämer, svampkrämer, antibiotika och de flesta receptfria topiska produkter) kan man göra ett korrekt val av det bästa alternativet för patienten.
Washington C, Washington N. Drug delivery to the skin. I: Physiological Pharmaceutics, Biological Barriers to drug absorption. 1st Ed Ellis Horwood 1989:109-120
Marjukka Suhonen TA, Bouwstra J. Chemical enhancement of percutaneous absorption in relation to stratum corneum structural alterations. J Control Release 1999:59:149-161
Ellias PM. Epidermala lipider, membran och keratinisering. Int J Dermatol 1981:20:1-19
Michaels AS, Shaw JE. Permeation av läkemedel genom mänsklig hud: Teori och experimentell in vitro-mätning. AIChE J 1975:21:985-996
Barry BW. Lipidproteinfördelningsteori för förbättrad hudpenetration. J Control Release 1991:15:237-248
Roberts MS. Riktad läkemedelsleverans till huden och djupare vävnader; fysiologins, lösningsstrukturens och sjukdomens roll. Clin Exp Pharmacol Physiol 1997:24:874-9
Scheuplein RJ. Hudens permeabilitet. Physiol Rev 1971:51:702-747
Mitragotri S. Breaking the skin barrier. Adv Drug Deliv Rev 2004:56:555-716
Barry BW. Nya mekanismer och anordningar för att möjliggöra framgångsrik transdermal läkemedelstillförsel. Eur J Pharm Sci 2001:14:101-114
Garavito MR. Detergenter som verktyg för membranbiokemi. J Biol Chm 2001:276:32403-6